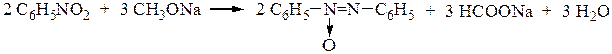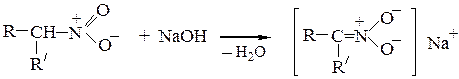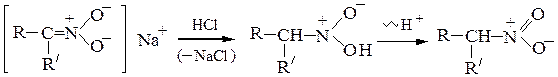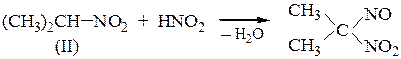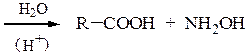Химические свойства.
1). Восстановление (каталитическое гидрирование, использование комплексных гидридов металлов – LiAlH4 (алюмогидрид лития), NaBH4 (боргидрид натрия) ) нитросоединений приводит к образованию первичных аминов:
(CH3)2СH–NO2 + 3 H2 ¾® (CH3)2СH–NH2 + 2 H2O (Ni) Аналогично нитроалканам каталитическое гидрирование, восстановление растворяющимся металлом или действие восстановителем в кислой среде приводит к образованию соответствующих ароматических первичных аминов
анилин
При восстановлении ароматических нитросоединений в щелочной среде в зависимости от условий реакции можно выделить ряд промежуточных продуктов. Так, при восстановление нитробензола до анилина в кислой среде протекает через стадии образования нитрозобензола и фенилгидроксиламина. В щелочной среде эти соединения конденсируются с образованием азоксибензола, а затем и продуктов более глубокого восстановления - азобензола и гидразобензола. При полном восстановлении нитробензола в кислой среде образуется анилин. Впервые анилин синтезирован Н.Н. Зининым при восстановлении сероводородом:
C6H5NO2 + 3 H2S —¾® C6H5NH2 + 2 Н2О + 3 S
Сегодня анилин получают из нитробензола с использованием в качестве восстановителей железа, цинка или олова в НС1, гидросульфида аммония и водорода или гидразина на никелевом катализаторе:
C6H5NO2 + 3 Zn + 6НС1 ¾¾® C6H5NH2 + 3 ZnCl2 + 2H2O
При восстановлении нитробензола в мягких условиях [цинковая пыль в водном растворе или пентакарбонил железа Fe(CO)5] процесс останавливается на стадии образования нитрозобензола. Восстановление нитробензола в слабокислой среде с использованием цинка в растворе хлорида аммония выделяется N-фенилгидроксиламин:
C6H5NO2 + 2 Zn + 4 NH4C1 ¾¾® C6H5NHOH + 2 [Zn(NH3)2]Cl2 + H2O
Восстановление нитробензола в щелочной среде приводит к образованию азоксибензола, азобензола и гидразобензола. Так, при восстановлении нитробензола метилатом натрия выделяется азоксибензол:
Действием алюмогидридом или станнитом натрия на нитробензол получают азобензол:
2C6H5NО2 + 4Na2SnO2 ¾¾® C6H5-N= N-C6H5 + Na2SnO3 + 8NaOH
Более глубокое восстановление до гидразобензола наблюдается при использовании цинковой пыли в щелочной среде:
2C6H5NO2 + 5Zn + 5NaOH + Н2О ¾® C6H5-NH-NH-C6H5 + 5NaHZnО2 2).Реакции, связанные с подвижностью α-атомов водорода. Характерны только для первичных и вторичных нитроалканов. а) Первичные и вторичные нитроалканы конденсируются в присутствии щелочей с альдегидами (например, с формальдегидом), образуя нитроспирты (реакция Генри).
Реакция протекает как нуклеофильное присоединение по карбониль-ному атому углерода, причем роль метиленовой компоненты конденсации (a-карбаниона) выполняет нитросоединение б) Действие щелочей. Первичные и вторичные нитросоединения растворяются в водных растворах щелочей с образованием солей, так как атомы водорода при a-углеродном атоме, связанном с очень сильным электроноакцептором - нитрогруппой, обладают кислотной подвижностью
При подкислении раствора сначала образуется аци-нитросоединение (нитроновая кислота), которая затем перегруппировывается в исходное нитросоединение:
Нитросоединения относятся к псевдокислотам – нейтральным соединениям, способным образовывать соли. Третичные нитросоединения со щелочами не реагируют. в) Первичные нитросоединения с азотистой кислотой образуют нитроловые кислоты:
вторичные нитросоединения образуют псевдонитролы:
3). Реакции с минеральными кислотами. При нагревании первичных нитроалканов с минеральными кислотами образуются карбоновые кислоты и соли гидроксиламина:
CH3CH2NO2 + HCl + H2O ¾¾® CH3COOH + HONH2 · HCl гидрохлорид гидроксиламина CH3CH2NO2 + H2SO4 ¾¾® CH3COOH + HONH2 · H2SO4 сульфат гидроксиламина
При обработке первичных или вторичных нитросоединений разбавленными минеральными кислотами образуются альдегиды или кетоны соответственно (реакция Нефа).
H2SO4 (t) 2 CH3CH2NO2 ¾¾¾¾® 2 CH3CHO + N2O + H2O ацетальдегид АМИНЫ
|