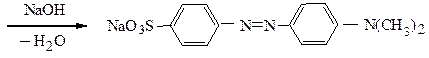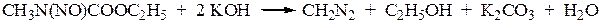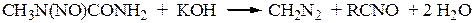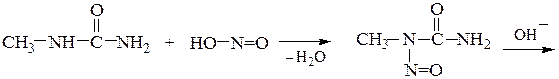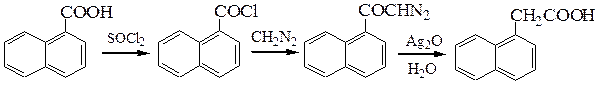Соли диазония.
Способ получения ароматических диазосоединений (солей диазония) из первичных ароматических аминов и смеси нитрита натрия и минеральной кислоты называется диазотированием. Поскольку эта реакция экзотермичная, а образующиеся соли диазония при нагревании разлагаются, то реакционная смесь охлаждается до 0-10 °С добавлением льда в реакционную массу.
ArNH2 + NaNO2 + 2 HCl ¾® ArN2+X- + NaCl + 2 H2O
Конец диазотирования определяется по посинению бумаги, пропитанной растворами KI и крахмала (йодо-крахмальная бумага). Азотистая кислота, находящаяся в избытке, окисляет I- до свободного иода, вызывающего появление характерной окраски крахмала.
Соли диазония готовят непосредственно перед использованием. Повышение температуры способствует их распаду с выделением азота и отражается на чистоте и выходе продуктов дальнейших превращений. Избыток азотистой кислоты нежелателен, так как возможно нитрозирование азосоставляющей и конкуренция с реакцией азосочетания. Его можно устранить добавлением в реакционную массу после диазотирования сухой мочевины или сульфаминовой кислоты до прекращения выделения газов:
Электронодонорные заместители, увеличивающие электронную плотность в ароматическом ядре, стабилизируют арилдиазоний-катион. Диазониевая группа легко замещается на другие функциональные группы с образованием ароматических веществ различных классов, а также на атом водорода, приводящий к ее элиминированию (см. Схему). Во всех реакциях выделяется азот, последняя реакция завершает цепь превращений, в которых используется ориентирующее действие нитро- или аминогруппы, превращающуюся затем в диазониевую. Этим нередко пользуются, учитывая доступность солей диазония и то, что пониженная реакционная способность арилгалогенидовв реакциях нуклеофильного замещения атома галогена ограничиваетприменение последних для синтеза производных ароматического ряда. Рассмотрим несколько примеров синтеза ароматических соединений использующие свойства солей диазония.
Пример 1. Синтез п -йодтолуола из п -толуидина:
Пример 2. Синтез о -броманизола из о -нитроанилина:
Пример 3. Синтез 3,4,5-трийод-1-нитробензола из 4-нитроанилина:
Схема. Синтезы на основе солей диазония.
Для получения азокрасителей используют реакции солей диазония с ароматическими фенолами и аминами (реакция азосочетания). Реакция азосочетания является реакцией электрофильного замещения (SE.), так как электроноакцепторные группы увеличивают, а электронодонорные группы снижают реакционную способность арилдиазоний-катиона. Электрофильный характер азосочетания подтверждается и тем, что при увеличении электронодонорности заместителей в ароматическом ядре скорость реакции возрастает. Ароматические соединения, не содержащие в ядре сильных электронодонорных заместителей, как правило, не могут выступать в роли азокомпонентов
В сильнокислой среде (рН < 5) возможно протонирование групп азокомпонентов (-ОН, -NR2), обусловливающих их повышенную реакционную способность; при этом азокомпоненты утрачивают свою способность к азосочетанию:
При рН > 10 из диазосоставляющей образуется диазотат-анион, не обладающий электрофильными свойствами:
Фенолы наиболее активны в роли азокомпонентов в реакциях азосочетания в форме фенолят-аниона, а амины - в непротонированной форме. При азосочетании возможны следующие побочные реакции: – разложение диазосоединения с выделением азота, скорость процесса при этом возрастает с повышением температуры и рН среды; – переход диазосоединения в неактивный диазотат-анион Ar-N=N-О- (обычно в сильнощелочной среде); – образование диазоаминосоединения при использовании в качестве азосоставляющего компонента амина. Реакция может быть основной при диазотировании недостатком азотистой кислоты в нейтральной или щелочной среде:
диазоаминобензол
Ниже приведены примеры получения азокрасителей из ароматических аминов путем превращения их в соли диазония (реакция диазотирования) и последующим взаимодействием ее с ароматическими фенолами или аминами (реакция азосочетания):
Пример 1. Получение 2-нафтолоранжа из сульфаниловой кислоты.
реакция диазотирования
Пример 2. Получение метилоранжа из сульфаниловой кислоты.
реакция диазотирования
(II)
В зависимости от рН среды азокрасители приобретают различную окраску, Так, индикаторные свойства метилоранжа обусловлены таутомерией: в щелочной среде он желтого цвета (бензоидная форма – II), в кислой - красного (хиноидная форма – I).
.
Алифатические диазосоединения. Важное значение в синтетической практике имеет диазометан. Строение диазометана может быть описано рядом резонансных структур:
Диазометан получают обработкой спиртовым раствором КОН эфирного раствора N-нитрозометилуретана
N-нитрозо-N-метил-п-толуолсульфамида:
N-нитрозометилмочевины (ниже приведен механизм этой реакции):
Диазометан легко метилирует соединения, содержащие активный атом водорода (с галогеноводородами дает метилгалогениды, с карбоновыми кислотами, сульфокислотами и фенолами - их метиловые эфиры). Метилирование органических соединений связано с его способностью легко давать диазониевый катион:
В прис. AlCl3 (или BF3) диазометан реагирует с альдегидами образуя метилкетоны. Также он способен к расширению цикла в циклических кетонах. C диазометаном обычно работают в растворах (эфир, бензол). Диазометан используют в синтезе Арндта-Эйстерта, позволяющем удлинять цепь углеродных атомов в молекуле карбоновой кислоты. Ниже приведена схема синтеза α-нафтилуксусной кислоты из α-нафтойной кислоты:
|

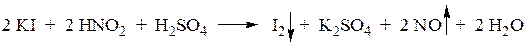


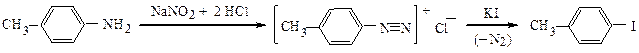
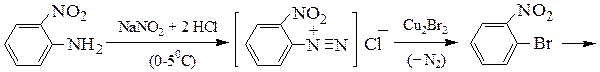
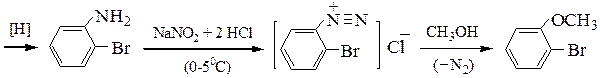
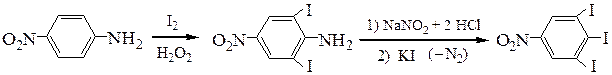

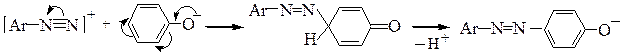


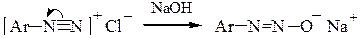
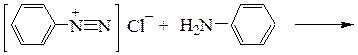

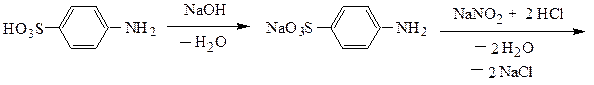
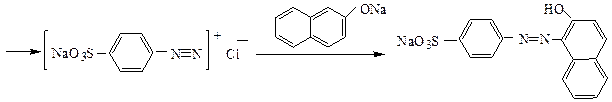 диазониевая соль реакция азосочетания 2-нафтолоранж
диазониевая соль реакция азосочетания 2-нафтолоранж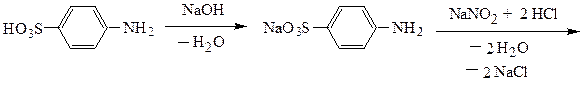
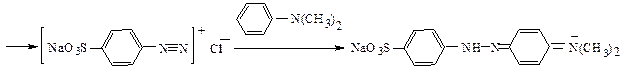 реакция азосочетания (I)
реакция азосочетания (I)