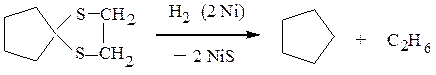Химические свойства. 1. Меркаптаны обладают более сильными кислотными свойствами, чем спирты и фенолы
1. Меркаптаны обладают более сильными кислотными свойствами, чем спирты и фенолы. Тиоспирты реагируют со щелочами, а также оксидами тяжелых металлов, образуя меркаптиды: 2. СH3CH2CH2SH + NaOH → CH3CH2CH2SNa + H2O
2 CH3CH2SH +HgO → (CH3CH2S) 2Hg + H2O
Меркаптиды можно алкилировать и ацилировать:
СH3CH2SNa + CH3I → СH3CH2 – S – CH3 + NaI метилэтилсульфид
СH3CH2SNa + CH3СOCl → СH3COSСH2CH3 + NaI этилтиоацетат
2. Тиоспирты значительно активнее, чем обычные спирты, реагируют с альдегидами и кетонами, образуя тиоацетали и тиокетали:
диэтилтиоацеталь бензальдегида
этилентиокеталь циклопентанона
Гидрирование циклических тиокеталей на никеле – удобный способ восстановления кетонов, а также удаления органической серы из угле-водородов, так называемое, обессеривание.
3. Меркаптаны легко окисляются. Такие слабые окислители, как серная кислота, йод и даже кислород воздуха, окисляют их до дисульфидов:
2 R – SH + I2 → R – S – S – R + 2 HI Сильные окислители превращают меркаптаны в сульфокислоты:
C2H5SH + K2Cr2O7 → C2H5SO3H этансульфокислота
|