Характеристичне рентгенівське випромінювання, його природа. Закон Мозлі.
Характеристичний спектр виникає тому, що частина бомбардуючих електронів проникає в атоми антикатода і збуджує їх. Причому електронні переходи відбуваються в надрах атомів, тобто в оболонках, ближчих до ядра – К, L, М. Тому енергія квантів рентгенівських променів більша від енергії квантів видимого світла, так як останні одержуються при електронних переходах між зовнішніми оболонками атома, тобто на його периферії.
Мал. 10.3. Розподіл інтенсивності по спектру випромінювання рентгенівської трубки з вольфрамовим анодом. Характеристичне випромінювання має лінійчастий спектр. Свою назву воно дістало тому, що цей тип рентгенівського випромінювання характеризує речовину антикатода і його вид не залежить від того, чи елемент знаходиться у вільному або хімічно зв’язаному стані. Характеристичні лінії завжди виникають на фоні неперервного спектра. На мал. 10.3 зображено графік розподілу інтенсивності по спектру випромінювання рентгенівської трубки з вольфрамовим анодом при Uа = 168 кВ. Цей графік наочно ілюструє той факт, що загальний спектр включає в себе як неперервний спектр, так і характеристичні лінії К -серії. На ділянці неперервного спектра, розміщеного зліва від накладених на нього спектральних ліній, видний “провал”. Ця відсутня енергія пішла на збудження сусідніх спектральних ліній.
Переходи, що закінчуються на L -оболонці та М -оболонці, дають відповідно L -серію і М -серію характеритичного рентгенівського спектра. Характеристичний спектр складається із 8–10 ліній, що утворюють К, L, Μ; серії. Для важких елементів в кожну серію входять три лінії α;, β;, γ;. Найінтенсивніша в характеристичному спектрі
Закон Мозлі. В 1913 р. англійський фізик Мозлі, досліджуючи залежність довжини хвилі характеристичних променів від атомного номера Ζ; різних елементів, встановив співвідношення, які називаються законом Мозлі:
де На мал. 10.5 зображено так звану діаграму Мозлі, яка ілюструє для ліній
|


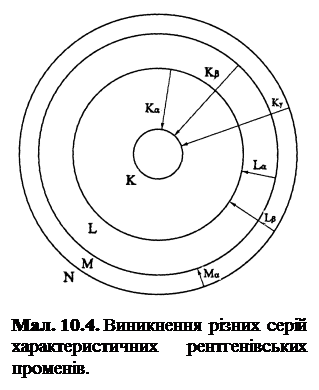 На мал. 10.4 схематично зображено виникнення різних серій характеристичних рентгенівських променів. В атомах з більшим атомним номером внутрішні електронні оболонки Κ;, L, Μ; повністю заповнені електронами. При вилученні електрона з однієї із внутрішніх оболонок на звільнене місце переходить електрон з більш віддаленої від ядра оболонки і випромінюється рентгенівський квант. Переходи, що закінчуються на К -оболонці, дають К -серію характеристичного спектра, яка складається з трьох ліній:
На мал. 10.4 схематично зображено виникнення різних серій характеристичних рентгенівських променів. В атомах з більшим атомним номером внутрішні електронні оболонки Κ;, L, Μ; повністю заповнені електронами. При вилученні електрона з однієї із внутрішніх оболонок на звільнене місце переходить електрон з більш віддаленої від ядра оболонки і випромінюється рентгенівський квант. Переходи, що закінчуються на К -оболонці, дають К -серію характеристичного спектра, яка складається з трьох ліній: – відповідає переходу з L -оболонки на К -оболонку,
– відповідає переходу з L -оболонки на К -оболонку, – відповідає переходу з М -оболонки на К -оболонку,
– відповідає переходу з М -оболонки на К -оболонку, – відповідає переходу з N -оболонки на К -оболонку.
– відповідає переходу з N -оболонки на К -оболонку.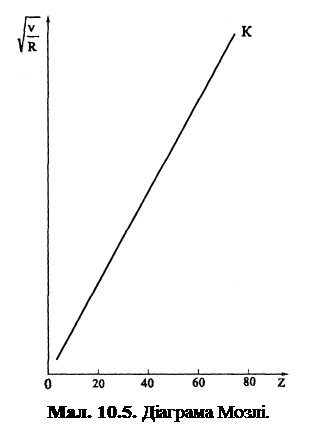 Для кожного атома існує межа збудження К -серії. Наприклад, для ртуті (
Для кожного атома існує межа збудження К -серії. Наприклад, для ртуті ( ) вона становить біля 82 кеВ. Це зв’язано з тим, що для виривання електрона із найближчої до ядра К -оболонки, на якій електрони найсильніше притягуються до ядра, необхідна значна енергія, яка іде на виконання роботи по вириванню електрона. Тому лінії характеристичного спектра з’являються тільки при напрузі на рентгенівській трубці, яка більша певного значення для кожного матеріалу анода.
) вона становить біля 82 кеВ. Це зв’язано з тим, що для виривання електрона із найближчої до ядра К -оболонки, на якій електрони найсильніше притягуються до ядра, необхідна значна енергія, яка іде на виконання роботи по вириванню електрона. Тому лінії характеристичного спектра з’являються тільки при напрузі на рентгенівській трубці, яка більша певного значення для кожного матеріалу анода. для К a-лінії, (10.4)
для К a-лінії, (10.4) для L -cерії,
для L -cерії, – стала Рідберга, σ; – постійна величина, яка зветься сталою екранування (для лінії
– стала Рідберга, σ; – постійна величина, яка зветься сталою екранування (для лінії  від атомного номера Z. Послідовне застосування формули Мозлі до елементів періодичної системи Менделєєва підтвердило в свій час закономірне зростання на одиницю заряду ядра при переході від одного елемента до наступного. Це стало природничо-науковим підтвердженням справедливості ядерної моделі атома і періодичного закону Д.І. Менделєєва.
від атомного номера Z. Послідовне застосування формули Мозлі до елементів періодичної системи Менделєєва підтвердило в свій час закономірне зростання на одиницю заряду ядра при переході від одного елемента до наступного. Це стало природничо-науковим підтвердженням справедливості ядерної моделі атома і періодичного закону Д.І. Менделєєва.


