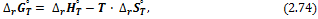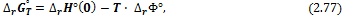Расчет изменения энергии Гиббса и Гельмгольца для различных процессов
1) Изменение энергий Гиббса и Гельмгольца при изменении температуры Температурная зависимость энергий Гиббса и Гельмгольца от температуры определяется соотношениями:
И в интегральной форме:
2) Изменение энергий Гиббса и Гельмгольца при изотермическом расширении или сжатии Изменения энергий Гиббса и Гельмгольца при сжатии или расширении, когда Т = const, выражаются в дифференциальной форме уравнениями:
Для идеальных газов в интегральной форме:
Для конденсированных систем при умеренных давлениях
где 3) Изменение энергий Гиббса и Гельмгольца при фазовых превращениях Изменение энергии Гиббса для фазовых переходов для испарения и возгонки (р = const) для плавления и полиморфных превращений 4) Изменение энергий Гиббса и Гельмгольца при химической реакции Рассмотрим различные способы: I. Изменение энергии Гиббса можно рассчитать, используя стандартные энергии Гиббса образования реагентов и продуктов:
II. По определению, G = H – TS:
где При произвольной температуре изменение энергии Гиббса рассчитывают аналогично:
при этом температурные зависимости стандартной энтальпии и энтропии реакции определяются выражениями (1.26) и (2.25) соответственно. III. Для расчета энергии Гиббса реакции удобно использовать так называемую приведенную энергию Гиббса или Ф-потенциал:
Приведенный потенциал имеет размерность [Дж·моль-1·К-1], численные значения этой функции для интересующего вещества при разных температурах можно найти в специализированных термодинамических справочниках. Для расчета стандартной энергии Гиббса реакции с помощью Ф-потенциала используют формулы:
Изменение энергии Гельмгольца химической реакции связано с энергией Гиббса соотношением
где Δ n – изменение количества молей газообразных веществ в ходе реакции. Для реакций в конденсированной фазе эти две величины практически одинаковы
|


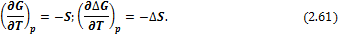




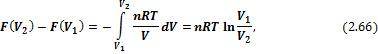


 – объем конденсированной фазы.
– объем конденсированной фазы.




 и
и  рассчитываем по уравнениям (1.16) и (1.18) соответственно.
рассчитываем по уравнениям (1.16) и (1.18) соответственно.