Химический потенциал
При протекании химической реакции меняется число и вид частиц (молекул). Поэтому термодинамические потенциалы будут функциями не только своих естественных переменных, но и числа молей компонентов системы ni. Тогда энергия Гиббса есть функция G = f (T, р, n 1, n 2 ,…), полный дифференциал которой равен
Обозначим
Величина Одно и тоже значение химического потенциала i -го компонента можно получить из зависимостей от числа молей ni термодинамических потенциалов при постоянных естественных переменных:
С учетом введенных обозначений выражения для полных дифференциалов термодинамических потенциалов имеют вид:
Соответственно получаем
В выражении (2.88) знак равенства соответствует установлению термодинамического равновесия, знак «меньше» – самопроизвольному протеканию химической реакции. Для того чтобы модно было использовать химический потенциал при решении практических задач, необходимо установить вид его зависимости от измеримых термодинамических переменных – температуры, давления и состава: – Идеальные газовые смеси:
где – Реальные газовые смеси:
где – Идеальные конденсированные растворы:
где – Реальные конденсированные растворы:
где
В нашем случае активность безразмерная величина. Также она может быть выражена через молярную или моляльную концентрации (активность будет иметь размерность концентрации), тогда будут изменяться значения коэффициентов активности. Коэффициенты активности – безразмерные величины, они характеризуют работу, которую надо совершить при перемещении i -го компонента из идеального раствора в реальный при постоянной температуре, давлении и концентрации.
|

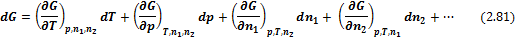

 – называется химическим потенциалом и представляет собой частную производную термодинамических потенциалов по количеству i -го компонента при фиксированных естественных переменных, т. е. он показывает, насколько изменяется соответствующий термодинамический потенциал при добавлении бесконечно малого количества i -го компонента к 1 молю раствора. Размерность Дж/моль.
– называется химическим потенциалом и представляет собой частную производную термодинамических потенциалов по количеству i -го компонента при фиксированных естественных переменных, т. е. он показывает, насколько изменяется соответствующий термодинамический потенциал при добавлении бесконечно малого количества i -го компонента к 1 молю раствора. Размерность Дж/моль.

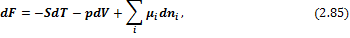




 – стандартный химический потенциал i -го газа, т. е. его потенциал в состоянии чистого вещества при заданной температуре и давлении 1 бар;
– стандартный химический потенциал i -го газа, т. е. его потенциал в состоянии чистого вещества при заданной температуре и давлении 1 бар;  – текущее парциальное давление газа.
– текущее парциальное давление газа.
 – летучесть или фугитивность – давление, которое должна производить реальная система, чтобы оказывать такое же действие, как идеальная система;
– летучесть или фугитивность – давление, которое должна производить реальная система, чтобы оказывать такое же действие, как идеальная система; 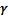 – коэффициент летучести используется для характеристики отклонения от идеального поведения.
– коэффициент летучести используется для характеристики отклонения от идеального поведения.
 – мольная доля компонента в смеси.
– мольная доля компонента в смеси.
 – активность, которая может быть представлена в виде произведения мольной доли
– активность, которая может быть представлена в виде произведения мольной доли  :
:



