Расчет изменения энтропии процессов расширения и сжатия идеального газа при различных условиях
Если в системе, состоящей из идеального газа, изменяется несколько параметров, то, например, для изобарно-изотермического процесса:
4) Смешение идеальных газов при постоянных температуре и давлении Если n 1 молей одного газа, занимающего объем V 1, смешиваются с n 2 молями другого газа, занимающего объем V 2, то общий объем будет равен V 1 + V 2, причем газы расширяются независимо друг от друга и занимают весь объем, поэтому общее изменение энтропии равно сумме изменений энтропии каждого газа:
где 5) Изменение энтропии при химической реакции При постоянной температуре и давлении изменение энтропии может быть рассчитано как термодинамическая сумма мольных абсолютных стандартных энтропий веществ, участвующих в реакции:
Изменение энтропии в ходе химической реакции при произвольной температуре рассчитывают по уравнению:
Изменение энтропии изолированной системы включает в себя два слагаемых: изменение энтропии процесса (Δ S пр.) и изменение энтропии теплового источника (Δ S т.ист.), который входит в систему для исключения возможности обмена ее энергией с окружающей средой. Тогда:
Важно отметить, что только эта суммарная величина позволяет предвидеть направление самопроизвольного процесса. Статистическое определение энтропии основано на идее о том, что необратимые процессы в термодинамике вызваны переходом системы в более вероятное состояние, поэтому энтропию можно связать с вероятностью:
где k – постоянная Больцмана (k = R / N A), W – так называемая термодинамическая вероятность, т.е. число микросостояний, которые соответствуют данному макросостоянию системы. Формулу (2.27) называют формулой Больцмана. Вероятность W какого-либо состояния равняется числу всех возможных сочетаний, посредством которых может быть реализовано данное состояние. С увеличением количества молекул и числа доступных уровней энергии термодинамическая вероятность резко увеличивается, так что для обычных молекулярных систем при повышении температуры и разупорядоченности энтропия возрастает. Верно и обратное. Во многих случаях изменение энтропии процесса можно оценить качественно, основываясь на следующих соображениях:
2.
|

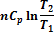

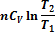


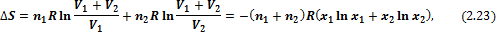
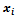 – мольная доля i -го газа в полученной газовой смеси. Изменение энтропии (3.23) всегда положительно, так как все
– мольная доля i -го газа в полученной газовой смеси. Изменение энтропии (3.23) всегда положительно, так как все  , поэтому идеальные газы всегда расширяются необратимо.
, поэтому идеальные газы всегда расширяются необратимо.

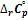 можно выразить как функцию температуры, используя температурные ряды теплоемкости; если известны средние теплоемкости
можно выразить как функцию температуры, используя температурные ряды теплоемкости; если известны средние теплоемкости  можно вынести за знак интеграла.
можно вынести за знак интеграла.




