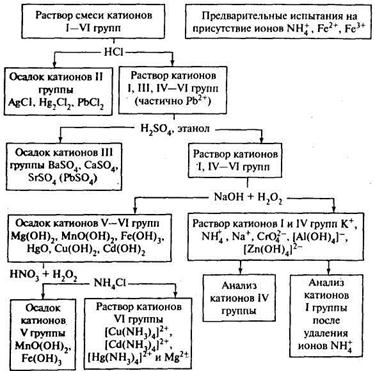
Систематический анализ смеси катионов всех аналитических групп
1. Предварительные испытания. В отдельных порциях исходного раствора дробным методом определяют ионы Fe2+, Fe3+ и NH+4. Ионы Са2+, Mg2+, Mn2+ и Na+ рекомендуется также определять дробным методом. Обнаружение Fe2+. К раствору, подкисленному соляной кислотой (1: 3), добавляют каплю раствора гексацианоферрата (III) калия K3[Fe(GN)6]. Образование темно-синего осадка указывает на присутствие Fe2+. Обнаружение Fe3+. К раствору, подкисленному соляной кислотой (1: 3), добавляют каплю раствора гексациазоферрата (II) калия K4[Fe(CN)6]. Появление синего осадка свидетельствует, о присутствии в растворе иона Обнаружение NH+4. В газовую камеру (см. рис. 7.8) вносят каплю исследуемого раствора, добавляют щелочь и быстро накрывают сверху часовым стеклом, на котором лежит влажная лакмусовая бумажка. Выделяющийся аммиак окрашивает лакмусовую бумажку в синий цвет. Обнаружение иона NH+4 можно провести и с помощью реактива Несслера, который дает желтую окраску раствора или красно-бурый осадок в присутствии солей аммония. Обнаружение Мn2+. Ионы марганца (II) обнаруживают в растворе с помощью персульфата аммония (§ 12.3). Обнаружение Са2+. Анализируемый раствор подкисляют серной кислотой. Образующийся осадок отделяют от раствора центрифугированием. Помещают каплю центрифугата на предметное стекло, упаривают до образования белого осадка и рассматривают под микроскопом. В присутствии ионов кальция Са2+ образуются характерные кристаллы в форме игл (см. рис. 10.1). Обнаружение Mg2+. К анализируемому раствору добавляют в избытке раствор гидроксида натрия. Тщательно перемешивают и центрифугируют. Осадок промывают два раза горячей водой, добавляют к осадку гидроксид аммония и хлорид аммония, тщательно перемешивают и центрифугируют. Реакцию обнаружения иона магния Mg2+ проводят на предметном стекле, соединяя капли центрифугата и раствора Na2HPO4. В присутствии ионов магния Mg2+ образуются кристаллы MgNH4PO4. Обнаружение Na+. К анализируемому раствору добавляют по каплям раствор карбоната калия до щелочной реакции. Центрифугируют. В растворе над осадком обнаруживают ион Na+ микрокристаллоскопической реакцией с фанилацетатом или гексагидроксостибиатом (V) калия см. §8.3). 2. Осаждение и анализ второй группы катионов. К раствору добавляют раствор соляной кислоты до прекращения образования осадка. Осадок анализируют, как описано в § 9. В растворе остаются катионы I, III, IV, V и VI групп. 3. Осаждение и анализ третьей группы катионов. После осаждения второй группы к раствору добавляют раствор серной кислоты в присутствии этанола и осадок анализируют как описано в § 10.5. После осаждения катионов третьей группы в растворе остаются катионы I, IV, V и VI групп. 4. Отделение и анализ катионов первой и четвертой групп. К раствору после осаждения катионов третьей группы добавляют избыток раствора гидроксида натрия с его массовой долей 10 %, а затем пероксид водорода, перемешивают и нагревают на водяной бане. Осадок образуют катионы пятой (Fe2+, Fe3+, Mn2+, Mg2+) и шестой (Cu2+, Hg2+, Cd2+) групп. В растворе остаются катионы первой (NH+4, К+, Na+) и четвертой (Zn2+, Al3+, Сr3+) групп. Раствор делят на две части. Одну часть анализируют на присутствие катионов четвертой группы, как указано в § 11.4. Другую часть раствора анализируют на присутствие катионов первой группы, как указано в § 8.4. 5. Анализ смеси катионов пятой и шестой групп. Осадок, содержащий катионы пятой и шестой групп, промывают 2-3 раза горячей водой в присутствии нитрата аммония. Затем осадок растворяют в азотной кислоте и пероксиде водорода. К полученному раствору добавляют избыток концентрированного раствора аммиака, несколько капель раствора хлорида аммония и пероксида водорода. Раствор тщательно перемешивают и нагревают, затем отделяют раствор от осадка. Раствор содержит аммиачные комплексные соли катионов шестой группы и катион Mg2+, так как при систематическом ходе анализа смеси катионов всех групп магний оказывается в растворе вместе с аммиакатами меди, ртути и кадмия. После осаждения Cu2S и HgS в присутствии тиосульфата натрия (см. § 13.4) в растворе остаются ионы магния Mg2+ и кадмия Cd2+. Катион магния Mg2+ обнаруживают реакцией с Na2HPO4 и NH4OH (см. § 12.3), а кати он кадмия Cd2+ - с помощью сероводорода или сульфида натрия (см. § 13.3). Оставшийся осадок содержит катионы пятой группы. Его промывают 2-3 раза разбавленным раствором аммиака и анализируют на присутствие катионов, как описано в § 12.4. Для наглядности ниже приводится схема анализа смеси катионов всех аналитических групп.
Рис. 13.1. Схема анализа смеси катионов I - VI групп (кислотно-основная классификация)
|