Распределительная хроматография
Распределительная хроматография основана на различии в растворимости разделяемых веществ в неподвижной фазе (газожидкостная хроматография) или на различии в растворимости веществ в подвижной и неподвижной жидких фазах. В последнем случае происходит перераспределение каждого вещества между двумя жидкими фазами в соответствии с его коэффициентом распределения К: K = C1 / C2 , (24.17)
где С1 - концентрация вещества в подвижной фазе; С2 -концентрация вещества в неподвижной фазе. Наибольшее применение для разделения, анализа и исследования веществ и их смесей, переходящих без разложения в парообразное состояние, получила газовая хроматография в обоих ее основных вариантах: газожидкостном и газотвердофазном (газоадсорбционном). В газовой хроматографии в качестве подвижной фазы (газа—носителя) используется инертный газ: гелий, азот, аргон, значительно реже водород и углекислый газ. В качестве адсорбентов (неподвижной фазы) применяют оксид алюминия, активированные угли или полимерные сорбенты. Газохроматографический процесс обычно осуществляют в специальных приборах, называемых газовыми хроматографами. Общая схема хроматографа приведена на рис. 24.9.
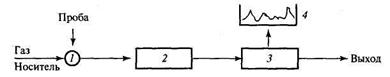
Рис. 24.9. Принципиальная схема газового хроматографа: 1 - устройство для ввода пробы в хроматографическую колонку (дозатор); 2 - хроматографическая колонка; 3 - детектор (анализирующая система); 4-регистратор
Поток газа-носителя из баллона непрерывно подается в хроматографическую колонку, а оттуда в детектирующее устройство. Оно непрерывно измеряет концентрацию компонентов у выхода из колонки и преобразует ее в электрический сигнал, регистрируемый потенциометром. На
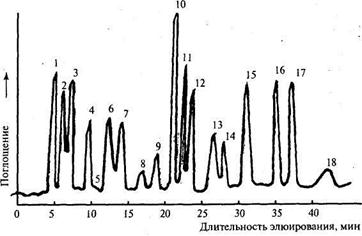
Рис. 24.10. Хроматограмма искусственной смеси аминокислот, входящих в состав продуктов гидролиза белков: 1 - аспарагиновая кислота; 2- треонин; 3 - серии; 4 - глютаминовая кислота; 5 - пролин; 6 - глицин; 7 - аланин; 8- цистин; 9 - валин; 10 - метионин; 11 - изолейцин; 12 - лейцин; 13 - тирозин; 14 - фенилаланин; 15 - гистидин; 16 - лизин; 17 - аммиак; 18 - аргинин
ленте самописца получается выходная кривая, которую называют хроматограммоа (рис. 24.10). Полученная хроматограмма обычно представляет собой ряд пиков. Площадь пика пропорциональна количеству каждого компонента, а время выхода пика при постоянном режиме работы прибора (постоянная температура колонки и скорость газа-носителя) характеризует природу компонента. Таким образом, на одном приборе можно проводить не только разделение, но и качественный и количественный анализ смесей. Современный хроматограф может включать несколько колонок и различные детекторы, а также автоматическое устройство для подготовки и ввода пробы. Подсоединенный к хроматографу компьютер, имеющий запоминающее устройство и банк хроматографических данных, обеспечивает аналитика богатой информацией. Метод газохроматографического анализа очень чувствителен. Для его проведения часто вполне достаточно нескольких кубических миллиметров газа, долей микролитра жидкости или долей микрограмма твердого вещества. Газовая хроматография находит широкое применение в медицине для определения содержания многочисленных лекарственных препаратов, определения уровня жирных кислот, холестерина, стероидов и т.д. в организме больного. В методе тонкослойной хроматографии (ТСХ) неподвижная твердая фаза тонким слоем наносится на пластинку из стекла, алюминиевой фольги или полиэфирной пленки. В качестве сорбента в ТСХ применяют силикагели, оксид алюминия, крахмал, целлюлозу и другие вещества с высокой адсорбционной способностью. Выбор растворителя зависит от природы сорбента и свойств анализируемых соединений. Часто применяют смеси растворителей из двух или трех компонентов. Пробу анализируемой жидкости в виде пятна или полосы наносят на стартовую линию (а) в 2-3 см от края пластинки (рис. 24.11).
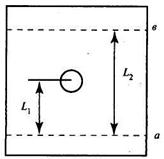
Рис. 24.11. Схема определения величины R при хроматографировании в тонком слое
Нанесение пробы осуществляют микропипетками, микрошприцами или специальными приспособлениями. Край пластинки погружают в растворитель (или систему растворителей), который действует как подвижная фаза. Под действием капиллярных сил растворитель движется вдоль слоя сорбента и с разной скоростью переносит компоненты смеси, что приводит к их разделению. Движение зон компонентов разделяемой смеси количественно характеризуется величиной R, которая называется индексом удерживания. За R принимают отношение расстояния L1, пройденного зоной вещества от стартовой линии до центра зоны, к расстоянию L2, пройденному растворителем за то же время (L2 равно расстоянию от стартовой линии до границы фронта растворителя (в) к концу опыта): Понятно, что L lне может быть больше L 2и значения R лежат в пределах от нуля до единицы. Стандартное вещество («свидетель») в том же растворителе наносится на стартовую линию рядом с анализируемой пробой и, таким образом, хроматографируется в тех же условиях. Влияние различных факторов на все вещества будет одинаковым, поэтому совпадение R компонента пробы и одного из «свидетелей» дает основания для отождествления веществ с учетом возможных наложений. Несовпадение R интерпретируется более однозначно, оно указывает на отсутствие в пробе соответствующего компонента. По окончании хроматографирования хроматограмму высушивают и проявляют химическим или физическим способом. При химическом способе пластинку опрыскивают раствором реактива, взаимодействующего с компонентами смеси. При обработке, например, парами йода четко проявляются органические соединения. В физических способах проявления используется способность некоторых веществ флуоресцировать под действием ультрафиолетового излучения. Вещества, обладающие радиоактивным излучением, обнаруживаются методом радиоавтографии с помощью различных фотоматериалов. Количественные определения в ТСХ могут быть сделаны или непосредственно на пластинке, или после удаления вещества с пластинки. При непосредственном определении на пластинке измеряют тем или иным методом площадь пятна (например, с помощью миллиметровой кальки) и по заранее построенному градуировочному графику находят количество вещества. Применяют также прямое спектрофотометрирование пластинки с помощью спектроденситометров. Наиболее точным считается метод, в котором вещество после разделения удаляется с пластинки и анализируется спектрофотометрическим или иным методом. В бумажной хроматографии в качестве носителя неподвижной жидкой фазы используется специальная хроматографическая бумага из чистой целлюлозы. Последняя содержит гидроксильные группы, которые удерживают возле себя полярный растворитель. Чаще всего это вода, которая играет роль неподвижной жидкой фазы. Органические растворители являются подвижной фазой. К ним обычно предъявляются следующие требования: растворители подвижной и неподвижной фаз не должны смешиваться, состав растворителя в процессе хроматографирования не должен изменяться, растворители должны легко удаляться с бумаги. При нанесении проб анализируемой смеси вещества, находящиеся в ней, увлекаются растворителем и одновременно происходит распределение компонентов смеси. Более полярные компоненты располагаются ближе к линии старта, неполярные компоненты продвигаются дальше. Таким образом можно провести качественно идентификацию различных соединений в присутствии стандартов («свидетелей») или по числовому значению R каждого компонента. По технике выполнения различают одномерную и двумерную бумажную хроматографию. Для получения двумерных хроматограмм хроматографирование производят дважды во взаимно противоположных направлениях: после обработки пробы одним растворителем хроматограмму поворачивают на 90° и хроматографируют вторично уже другим растворителем. Такая методика позволяет проводить более тонкие разделения компонентов смеси. Количественные определения, как и в ТСХ, выполняются по площади пятна и интенсивности его окраски. Нередко хроматограмму разделяют на отдельные части по числу пятен. Каждое пятно обрабатывают соответствующим органическим растворителем или смесью растворителей. Вещество, перешедшее в органический слой, определяют любым подходящим методом: фотометрическим, электрохимическим и др.
|