Зависимость скорости реакции от температуры
Скорость большинства химических реакций с повышением температуры возрастает. Это зависимость приближённо описывается эмпирическим правилом Вант-Гоффа: при повышении на каждые 10 градусов скорость химической реакции увеличивается в 2-4 раза. Математически правило Вант-Гоффа можно выразить следующей математической зависимостью:
где v1 – cкорость реакции при температуре t1; v2 – скорость реакции при температуре t2; γ – температурный коэффициент скорости, равный 2-4 для разных реакций. Более точно зависимость константы скорости от температуры описывается уравнением Аррениуса: k = P·Z·e где k – константа скорости реакции; Z – частота столкновений (число столкновений в единице объёма за единицу времени), измеряется в единицах константы скорости; R – газовая постоянная, кДж/моль∙ К; Т – абсолютная температура, К; Еа – энергия активации, кДж/моль. Под энергией активации понимают минимальный избыток энергии (по сравнению с величиной средней энергии молекул), которым должны обладать молекулы для того, чтобы реакция между ними стала возможной. Такие молекулы называются активными. Множитель e В уравнение Аррениуса введён также поправочный множитель Р (стерический фактор), учитывающий ориентацию сложных молекул в пространстве в момент столкновения по отношению друг к другу. Чем сложнее участвующие в реакции молекулы, тем меньше Р, а значит, и скорость реакции. Уравнение Аррениуса можно представить также в виде:
где k1, k2 – константы скорости соответственно при температурах Т1 и Т2. Уравнение (98) используют для вычисления константы скорости реакции при заданной температуре, если известна величина её для другой (близкой) температуры и величина Еа. Интервал температур Т1 и Т2 необходимо брать близким, так как в широком диапазоне Еа заметно изменяется. Можно также по двум константам скоростей, измеренным при двух близких температурах, вычислить энергию активации данной реакции.
Пример 14. Реакция между веществами А и В выражается уравнением 2А + В → С Начальная концентрация вещества А равна 3, 2 моль/л, а вещества В – 1, 6 моль/л. Константа скорости реакции 0, 75. какова скорость реакции в начальный момент и по истечении некоторого времени, когда концентрация вещества А уменьшилась на 0, 5 моль/л? Решение. Используем уравнение (86) для вычисления скорости реакции в начальный момент v0 = k · (с По истечении некоторого времени, когда концентрация вещества А уменьшится на 0, 5 моль/л, концентрация вещества В (в соответствии с уравнением химической реакции) должна уменьшится на 0, 25 моль, т.е. сВ = 1, 6 – 0, 25 = 1, 35 моль/л. Следовательно, скорость реакции станет равной v1 = k · (с v1 = 0, 75 · (2, 7)2 · 1, 35 = 7, 38.
Пример 15. Реакция разложения пероксида водорода в водном растворе протекает как реакция первого порядка. Период полураспада при данном условии равен 15, 86 мин. Определить, какое время потребуется для разложения (при заданных условиях) 99% пероксида водорода. Решение. По периоду полураспада, используя выражение (91), вычислим константу скорости разложения перикиси водорода: k = Зная константу, определяем время, за которое разложится 99% перекиси водорода: k =
Пример 16. Вычислить по правилу Вант-Гоффа, при какой температуре реакция закончится за 25 мин, если при 20º С на это требуется 2ч. Температурный коэффициент скорости реакции равен 3. Решение. Между константами скоростей и временем завершения реакции существует обратно пропорциональная зависимость
где τ 1 и τ 2 – время завершения реакции при температурах t1 и t2. Тогда уравнение (96) можно записать
откуда t2 – t1 = а t2 =
Пример 17. Для одной из реакций опытным путём были определены две константы скорости при 443º С – 0, 0067, а при 508º С – 0, 1059. Определить энергию активации данной реакции. Решение. Используя формулу (98), откуда получаем Еа = или Еа = Т1 = 443 + 273 = 716 К; Т2 = 508 + 273 = 781 К; R = 8, 314 Дж/(моль·К); Еа =
Вариант 1. 10. Рассчитайте среднюю скорость некоторой реакции, если за 10 мин концентрация реагента уменьшилась от 0, 05 моль/дм3 до 0, 01 моль/дм3.
11. При какой температуре период полупревращения равен 1 час, если энергия активации реакции равна 100 кДж/моль, а предэкспоненциальный множитель константы скорости равен 1013 с-1?
Вариант 2. 10. Для некоторой реакции при повышении температуры константа скорости изменяется следующим образом (табл.): Таблица
Найдите графическим и аналитическим методами энергию активации этой реакции.
11. Некоторая реакция при t=25º C завершается за 2 часа. через какое время закончится эта реакция при t=75º C, если её температурный коэффициент равен 2? Вариант 3.
10. Реакция взаимодействия триэтиламина с метилиодидом в растворе четырёххлористого углерода (C2H5)3N + CH3I → CH3(C2H5)3NI является реакцией второго порядка. При Т=293 К константа скорости реакции равна 2, 48·10-2дм3/(моль·мин). Начальные концентрации обоих реагентов равны 0, 224моль/дм3. Определить концентрацию триэтиламина через 5 часов после начала реакции.
11. Реакция разложения SO2Cl2: SO2Cl2 = SO2 + Cl2 является реакцией первого порядка. При 552 К константа скорости реакции равна 0, 609·10-4мин-1; а при 593 К – 13, 20·10-4 мин-1. Рассчитайте период полупревращения этой реакции при 688 К.
Вариант 4. 10. Реакция взаимодействия триэтиламина с метилиодидом в растворе четырёххлористого углерода (C2H5)3N + CH3I → CH3(C2H5)3NI является реакцией второго порядка. При Т=293 К константа скорости реакции равна 2, 48·10-2дм3/(моль·мин). Начальные концентрации обоих реагентов равны 0, 224моль/дм3. Определить время, в течение которого концентрация (C2H5)3N уменьшится в 1, 5 раза.
11. Для реакции первого порядка: N2O ↔ N2 + ½ O2 протекающей при температуре 1085 К, энергия активации равна 256, 75 кДж/моль, предэкспоненциальный множитель константы скорости реакции равен 1, 33·109 с-1. Определите время, в течение которого концентрация N2O изменится от 0, 21 моль/дм3 до 0, 07 моль/дм3. Вариант 5. 10. Для некоторой реакции первого порядка период полупревращения составляет 2 года. Сколько потребуется времени, чтобы концентрация исходного вещества уменьшилась в 10 раз?
11. Для реакции, протекающей по уравнению: СО + Н2О = СО2 + Н2 при 288 К константа скорости равна 0, 31·10-3 дм3/(моль·мин). Энергия активации равна 97, 06 кДж/моль. Чему будет равна константа скорости этой реакции при температуре 313 К?
Вариант 6. 10. Как изменятся скорости прямой и обратной реакции 4HCl + O2 ↔ 2 H2O(пар) + 2 Cl2 при увеличении давления в два раза и постоянной температуре?
11. При одинаковой концентрации реагирующих веществ скорость некоторой реакции, протекающей при 35º C, в два раза выше, чем при 25º C. Вычислить энергию активации данной реакции. Вариант 7. 10. Во сколько раз увеличится скорость прямой реакции 2SO2 + O2↔ 2SO3 протекающей в закрытом сосуде, если увеличить давление в пять раз без изменения температуры?
11. Для реакции первого порядка А → С период полупревращения при 450 К равен 40 мин. Предэкспоненциальный множитель константы скорости реакции равен 5, 4·1011с-1. Определить, чему равна величина энергии активации данной реакции. Вариант 8. 10. В закрытом сосуде находится смесь газов, состоящая из 1 моль азота и 3 моль водорода, которая реагирует по уравнению N2 + 3H2 ↔ 2NH3 Во сколько раз уменьшится скорость прямой реакции после того, как прореагирует 0, 65 моль азота?
11. Энергия активации реакции второго порядка, протекающей при температуре 627 К, 2NO2 = 2NO + O2 равна 111, 2 кДж/моль. Предэкспоненциальный множитель константы скорости реакции равен 3, 36·109 дм3/(моль·с). Начальная концентрация NO2 равна 0, 09 моль/дм3. Определите период полупревращения для этой реакции. Вариант 9. 10. разложение закиси азота на поверхности золота при высоких температурах протекает по уравнению N2O ↔ N2 + O Константа скорости данной реакции 0, 0005 при 900º С. начальная концентрация закиси азота 3, 2 моль/л. определить скорость реакции при указанной температуре в начальный момент и когда произойдёт разложение 78% закиси азота.
11. Константа скорости омыления уксусноэтилового эфира гидроксидом натрия при 282, 6 К равна 2, 37 дм3/(моль·мин), а при 287, 6 К – 3, 20 дм3/(моль·мин). При какой температуре константа скорости будет равна 4, 00 дм3/(моль·мин)? Вариант 10. 10. Реакция между веществами А и В протекает по уравнению А + 2В ↔ С Концентрация вещества А равна 1, 5 моль/л, а В – 3 моль/л. Константа скорости реакции 0, 4. Вычислить скорость химической реакции в начальный момент времени и по истечении некоторого времени, когда прореагирует 75% А.
11. Вычислить по правилу Вант-Гоффа, при какой температуре реакция закончится в течение 20 мин, если при 20º C на это требуется 3 ч. Температурный коэффициент скорости принять равным 2.
|

 , (96)
, (96) , (97)
, (97) , (98)
, (98) )2 · с
)2 · с  = 0, 75 · (3, 2)2 · 1, 6 = 12, 29.
= 0, 75 · (3, 2)2 · 1, 6 = 12, 29.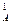 )2 · с
)2 · с 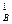 или
или .
. ;
;  ;
;
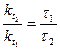 ,
, ,
,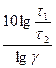 ,
,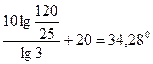 .
. ,
,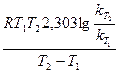 ,
, Дж/моль = 197, 5 кДж/моль.
Дж/моль = 197, 5 кДж/моль.


