Способы выражения концентрации растворов. .
Концентрация растворов – это есть содержание растворенного вещества (в молях или граммах) в определенном объеме или массе раствора или растворителя. Существуют следующие основные способы выражения концентрации растворов: 1) Массовая доля растворенного вещества – это есть отношение массы растворенного вещества к массе раствора, то есть:
Например, 5 г NaOH содержится в 50 г раствора. Тогда Необходимо помнить, что
где ρ – плотность раствора (г/мл); V – объем раствора (мл). 2) Молярная концентрация (или молярность) – это отношение количества растворенного вещества (n) к объему раствора (V) или число молей растворенного вещества в 1 литре раствора, т.е.:
где m – масса растворенного вещества М – молярная масса растворенного вещества (г/моль) V – объем раствора (л) Например, в 500 мл раствора содержится 19, 6 г H2SO4. Тогда, то есть в 1 литре раствора содержится 0, 4 моль серной кислоты. 3)Молярная концентрация эквивалента растворенного вещества – это есть отношение количества эквивалентов (число молей эквивалентов) растворенного вещества к объему раствора (или число молей эквивалентов растворенного вещества в 1 литре раствора), то есть: Сн = гдеМэ – молярная масса эквивалента растворенного вещества Например, в 100 мл раствора содержится 9, 8 г серной кислоты. Тогда Сн = то есть в 1 литре раствора содержится 2 моль эквивалентов серной кислоты, то есть получился двухнормальный раствор серной кислоты. 3) Моляльная концентрация (или моляльность) – это есть количество (число молей) растворенного вещества в 1 кг растворителя (или в 1000 г растворителя), то есть:
Например, в 200 г воды (то есть растворителя) растворено 4 г NaOH. Тогда 4) Молярная доля растворенного вещества – это отношение количества (числа молей) растворенного вещества к сумме количеств (к сумме молей) всех веществ, составляющих раствор, то есть:
Например, 8 г NaOH растворено в 14, 4 г воды. Тогда
Отсюда
то есть молярная доля NaOH в растворе равна 0, 2. 5) Титр раствора (Т) – это есть число граммов растворенного вещества в 1 мл раствора, то есть:
Например, в 100 мл раствора содержится 5 г серной кислоты. Тогда то есть в 1 мл раствора содержится 0, 05 г серной кислоты.
|

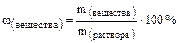


 ,
,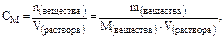

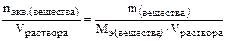
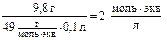 или 2н раствор Н2SO4
или 2н раствор Н2SO4

 то есть в 1 кг воды содержится 0, 5 моля NaOH.
то есть в 1 кг воды содержится 0, 5 моля NaOH.








