Типовая задача. Для растворения 16,8 г двухвалентного металла потребовалось 14,7 г серной кислоты
Для растворения 16, 8 г двухвалентного металла потребовалось 14, 7 г серной кислоты. Определить эквивалентную и атомную массы металла и объем выделившегося водорода (н.у.)
Решение. 1.Определить эквивалентную массу металла мы можем, воспользовавшись законом эквивалентов. Запишем его математическое выражение применительно к данной задаче:
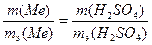 , где , где
m(Me) и m(H2SO4) – массы металла и кислоты, г;
mэ(Me) и mэ(H2SO4) - эквивалентные массы металла и кислоты, г/моль.
1. Эквивалентная масса кислоты определяется следующим отношением:
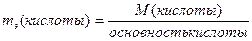 , где , где
М (кислоты) – молярная масса кислоты, г/моль.
Применительно к данной задаче

2. Подставляя значения в математическое выражение закона эквивалентов, получаем значение эквивалентной массы металла:
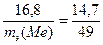 , отсюда , отсюда 
3. Чтобы определить атомную массу металла воспользуемся формулой:
 , где , где
Аr(Ме) и В(Ме) – это соответственно относительная атомная масса и валентность металла.
Отсюда 
4. Пользуясь законом эквивалентов, определяем объем выделившегося водорода:
 , где , где
V(H2) – объем водорода, л;
Vэ (H2) – эквивалентный объем водорода, л/моль.
Эквивалентный объем водорода при нормальных условиях равен 11, 2 л/моль

Ответ: mэ(Ме)=56 г/моль
Аr(Ме)=112 а.е.м.
V(H2)=3, 36 л
Варианты заданий
Таблица 1
| №
п/п
| Масса
металла, г
| Валентность металла
| Название кислоты
| Масса
кислоты, г
| |
|
|
|
|
| | 1.
| 8, 6
|
| Серная
| 15, 0
| | 2.
| 11, 7
|
| Соляная
| 18, 5
| | 3.
| 16, 6
|
| Ортофосфорная
| 27, 0
| | 4.
| 11, 8
|
| Соляная
| 25, 0
| | 5.
| 38, 3
|
| Ортофосфорная
| 32, 0
| | 6.
| 32, 9
|
| Серная
| 19, 0
| | 7.
| 27, 5
|
| Соляная
| 34, 0
| | 8.
| 35, 3
|
| Серная
| 13, 0
| | 9.
| 12, 0
|
| Ортофосфорная
| 17, 0
| | 10.
| 8, 2
|
| Соляная
| 15, 0
| | 11.
| 15, 4
|
| Серная
| 11, 0
| | 12.
| 35, 7
|
| Соляная
| 19, 0
| | 13.
| 9, 2
|
| Ортофосфорная
| 25, 0
| | 14.
| 14, 4
|
| Серная
| 24, 0
| | 15.
| 24, 0
|
| Соляная
| 27, 0
| | 16.
| 3, 8
|
| Серная
| 15, 6
| | 17.
| 3, 7
|
| Ортофосфорная
| 13, 2
| | 18.
| 10, 7
|
| Соляная
| 14, 0
| | 19.
| 1, 5
|
| Серная
| 8, 0
| | 20.
| 12, 9
|
| Ортофосфорная
| 15, 0
| | 21.
| 21, 1
|
| Серная
| 10, 0
| | продолжение табл. 1
| |
|
|
|
|
| |
|
|
|
|
| | 22.
| 13, 9
|
| Серная
| 21, 0
| | 23.
| 7, 6
|
| Соляная
| 31, 0
| | 24.
| 5, 9
|
| Серная
| 11, 5
| | 25.
| 13, 1
|
| Ортофосфорная
| 21, 3
| | 26.
| 29, 2
|
| Соляная
| 27, 4
| | 27.
| 10, 9
|
| Серная
| 19, 1
| | 28.
| 6, 6
|
| Ортофосфорная
| 18, 0
| | 29.
| 5, 9
|
| Соляная
| 24, 0
| | 30.
| 7, 0
|
| Серная
| 17, 2
|

Шрифт зодчего Шрифт зодчего состоит из прописных (заглавных), строчных букв и цифр...
|

Картограммы и картодиаграммы Картограммы и картодиаграммы применяются для изображения географической характеристики изучаемых явлений...
|

Практические расчеты на срез и смятие При изучении темы обратите внимание на основные расчетные предпосылки и условности расчета...
|

Функция спроса населения на данный товар Функция спроса населения на данный товар: Qd=7-Р. Функция предложения: Qs= -5+2Р,где...
|
Типовые ситуационные задачи. Задача 1.У больного А., 20 лет, с детства отмечается повышенное АД, уровень которого в настоящее время составляет 180-200/110-120 мм рт Задача 1.У больного А., 20 лет, с детства отмечается повышенное АД, уровень которого в настоящее время составляет 180-200/110-120 мм рт. ст. Влияние психоэмоциональных факторов отсутствует. Колебаний АД практически нет. Головной боли нет. Нормализовать...
Эндоскопическая диагностика язвенной болезни желудка, гастрита, опухоли Хронический гастрит - понятие клинико-анатомическое, характеризующееся определенными патоморфологическими изменениями слизистой оболочки желудка - неспецифическим воспалительным процессом...
Признаки классификации безопасности Можно выделить следующие признаки классификации безопасности.
1. По признаку масштабности принято различать следующие относительно самостоятельные геополитические уровни и виды безопасности.
1.1. Международная безопасность (глобальная и...
|
БИОХИМИЯ ТКАНЕЙ ЗУБА В составе зуба выделяют минерализованные и неминерализованные ткани...
Типология суицида. Феномен суицида (самоубийство или попытка самоубийства) чаще всего связывается с представлением о психологическом кризисе личности...
ОСНОВНЫЕ ТИПЫ МОЗГА ПОЗВОНОЧНЫХ Ихтиопсидный тип мозга характерен для низших позвоночных - рыб и амфибий...
|
|

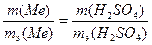 , где
, где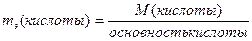 , где
, где
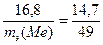 , отсюда
, отсюда 
 , где
, где
 , где
, где



