ТЕМА 4 АЛКИНЫ И АЛКАДИЕНЫ
Алкинами являются непредельными углеводородами, содержа-щими тройную связь. По названию первого члена этого гомологического ряда – ацетилена – их иногда называют ацетиленовыми углеводородами. Общая формула гомологического ряда алкинов СnH2n-2. Тройная связь, входящая в состав алкинов, состоит из одной σ -связи и двух π -связей.
Непредельные углеводороды могут содержать и две двойные связи. В этом случае их называют диеновыми углеводородами. Общая формула гомологического ряда алкадиенов CnH2n-2. Особый интерес представляют алкадиены с сопряженными двойными связями (соединения типа дивинила). В соединениях этого типа наблюдается взаимодействие π -электронов двойных связей, и вследствие их близкого нахождения друг к другу происходит образование единой π -системы, в которой π -электроны распределены по всей молекуле. Алкадиены, являясь непредельными углеводородами, проявляют склонность к реакциям присоединения. Однако, наличие в их составе двух π -связей обусловливает протекание реакций присоединения двумя путями. Основным направлением реакций присоединения к диеновым углеводородам являются реакции присоединения в положение 1, 4 (для дивинила – к концевым атомам углерода). 1. Гидрирование: t, Ni CH ≡ CH + Н2 → СН2 = СН2 → СН3 – СН3 ; СН2=СН–СН=СН2 + Н2 → СН3–СН=СН–СН3. Возможен и другой путь присоединения, когда реагент атакует одну из двойных связей и присоединяется по месту ее разрыва, оставляя вторую π -связь незатронутой (присоединение в 1, 2-положение): СН2=СН–СН=СН2 + Н2 → СН3–СН2–СН=СН2 .
Направление реакции присоединения зависит как от природы реагента, так и от условий реакции. 2. Галогенирование. В результате галогенирования получаются галогенопроизводные. При бромировании происходит обесцвечива-ние раствора брома, что служит качественной реакцией на кратную связь:
CH ≡ CH + 2Br2 → СНBr2 – СНBr2 тетрабромэтан; СН2=СН–СН=СН2 + Br2 → СН2Br–СН=СН–СН2Br. 1, 4-дибромбутен-2 3. Присоединение галогеноводородов. Эта реакция имеет большое практическое значение для получения мономера-винилхлорида, полимеризацией которого получают ценный полимерный материал, имеющий широкое применение в различных отраслях народного хозяйства:
CH ≡ CH + HCl → СН2 = СНCl хлористый винил; nСН2 = СНCl → [– СН2 – СНCl –]n поливинилхлорид.
Гомологи ацетилена присоединяют галогеноводороды в соот-ветсвии с правиломВ. В. Марковникова:
CH3 – С≡ CH + HBr → CH3 – СBr = CH2 2-бромпропен.
Реакции с алкадиенами:
СН2=СН–СН=СН2 + HBr → СН2Br–СН=СН–СН3. 1-бромбутен-2
4. Гидратация алкинов. Реакция гидратации ацетилена открыта в 1881 году М. Г. Кучеровым и поэтому часто носит его имя. Как было в дальнейшем установлено Эльтековым, вначале образуется не-устойчивый спирт с гидроксильной группой у углерода при двойной связи, который изомеризуется в уксусный альдегид (в случае гидратации ацетилена) или ке
H
OH O
СН ≡ CH + HCN → CH2 = CHCN;
CN 6. Присоединение уксусной кислоты. Винилацетат (виниловый эфир уксусной кислоты) получают из ацетилена и уксусной кислоты:
СН ≡ СН + СН3 – СООН → СН2 = СН – ОСОСН3.
Из винилацетата получают поливинилацетат:
n СН2 = СН – ОСОСН3 → – СН2 – СН –
ОСОСН3
7. Окисление. Ацетилен окисляется очень легко. При добавлении его в раствор перманганата калия происходит обесцвечивание послед-него, что используется для качественного определения алкинов.
СН ≡ СН + 2О2 → СО2 + НСООН муравьиная кислота.
8. Полимеризация. В зависимости от условий реакции ацетилен может димеризоваться (взаимно соединяются две молекулы):
СН ≡ СН + СН ≡ СН → СН2 = СН – С ≡ СН; винилацетилен либо тримеризоваться, превращаясь в бензол:
СН Одной из наиболее важных реакций является полимеризация алкадиенов, обычно протекающая по типу присоединения в 1, 4-поло-жение. В результате этой реакции образуется высокомолекулярные соединения, содержащие в своем составе двойную связь:
nСН2=СН–СН=СН2 → [СН2–СН=СН–СН2]n;
СН3 СН3 Углерод, связанный тройной связью, является более электроотрицательным по сравнению с углеродом, связанным одинарной или двойной связью. В результате водород, связанный с углеродом при тройной связи, обладает способностью замещаться щелочными или тяжелыми металлами с образованием ацетиленидов:
2 CH≡ CH + 2Na → 2CH≡ C–Na + H2 ацетиленид натрия.
Таким образом, в данном разделе представлены химические свойства нерпедельных углеводородов ‒ алкинов: гидрирование, галогенирование, присоединение галогеноводородов, гидратация алкинов, присоединение цианистого водорода, присоединение уксусной кислоты, окисление, полимеризация. [ 3, с. 34− 43; 5, с. 76− 82, 86− 94; 6, с. 414− 417].
|

 Являясь более ненасыщенными соединениями чем алкены, ацетиленовые углеводороды вступают в реакции присоединения, про-текающие за счет разрыва π -связей, причем присоединение реагентов происходит последовательно с разрывом каждой из π -связей.
Являясь более ненасыщенными соединениями чем алкены, ацетиленовые углеводороды вступают в реакции присоединения, про-текающие за счет разрыва π -связей, причем присоединение реагентов происходит последовательно с разрывом каждой из π -связей. тон (в случае гидратации гомологов ацетилена).
тон (в случае гидратации гомологов ацетилена).
 O
O CH ≡ CH + H2O → [CH2 = CHOH] → CH3 – C;
CH ≡ CH + H2O → [CH2 = CHOH] → CH3 – C;
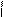
 CH3 – С ≡ CH + H2O → [CH3 – C = CH] → CH3 – C – CH3.
CH3 – С ≡ CH + H2O → [CH3 – C = CH] → CH3 – C – CH3. 5. Присоединение цианистого водорода. Данная реакция имеет практическое значение, т. к. из ацетилена получают акрилонитрил (нитрил акриловый кислоты), который превращают в полиакрило-нитрил:
5. Присоединение цианистого водорода. Данная реакция имеет практическое значение, т. к. из ацетилена получают акрилонитрил (нитрил акриловый кислоты), который превращают в полиакрило-нитрил: nCH2 = CH – CN → [– CH2 – CH –]n.
nCH2 = CH – CN → [– CH2 – CH –]n.
 n.
n.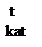

 СН
СН





 nСН2=С–СН=СН2 → [–СН2–С=СН–СН2]n.
nСН2=С–СН=СН2 → [–СН2–С=СН–СН2]n.



