ТЕМА 23 ДИАЗОСОЕДИНЕНИЯ. АЗОКРАСИТЕЛИ
Наибольшее практическое и препаративное значение в химии ароматических аминов имеет реакция с азотистой кислотой. По этой причине данную реакцию целесообразно рассматривать подробнее. Взаимодействие первичных ариламинов с азотистой кислотой называется диазотированием. Вследствие неустойчивости азотистой кислоты фактическим диазотирующим агентом является смесь соляной (или серной) кислоты и нитрита натрия, взаимодействии которых приводит к образованию NО+:
t0 = 00 + 50C
Реакция проводится при низких температурах, так как при более высоких диазосоединение разлагается с выделением азота. На один эквивалент амина берется не менее 2, 5 эквивалентов НСℓ или Н2SО4. Один эквивалент идет на выделение азотистой кислоты, один образует соль диазония, а оставшаяся часть стабилизирует эту соль. Образовавшаяся азотистая кислота в кислой среде разлагается по уравнению: Н
Механизм реакции диазотирования: НО − NО
НСℓ
НСℓ НСℓ
Н
При обработке холодного раствора соли диазония водным раствором КОН образуется несколько новых изомерных продуктов, между которыми устанавливается равновесие:
Аr − N = N − О − К+ диазотат калия (рН > 7) Следует отметить, что электрофильный ион диазония разрушается при щелочных значениях рН.
КОН
(кислая среда) гидроксид диазония
КОН диазокислота диазотат калия рН ≈ 7 рН > 7
Рассматривая химические свойства диазосоединений, необходимо акцентировать внимание на том, что наиболее реакционноспособными соединениями являются соли диазония. Вступая в целый ряд различных превращений, они позволяют вместо NН2 группы вводить в бензольное ядро разнообразные функции. Для солей диазония протекают два типа реакций: с выделением азота и без выделения азота. К реакциям первого типа относятся реакции разложения при кипячении кислых солей диазония, замещение диазогруппы на йод при нагревании их с КI. Удобным методом для получения ароматических соединений различных классов являются реакции, связанные с применением в качестве катализаторов соответствующих солей меди или медного порошка. Пример:
Z − сильная активирующая бензольное ядро группа (− ОН, − NН2, − ОСН3). В данном разделе рассмотрены химические свойства диазосоединений. [ 1, с. 142− 148; 2, с. 205; 4, с. 39− 45; 5, с. 428− 435].
|

 Аr − NН2 + 2 НСℓ + NаNО2 Аr − N ≡ NСℓ + NаСℓ + Н2О.
Аr − NН2 + 2 НСℓ + NаNО2 Аr − N ≡ NСℓ + NаСℓ + Н2О. ...... Н+ +....
...... Н+ +.... Н − О − N = О Н − О → Н2О + [N = О]+.
Н − О − N = О Н − О → Н2О + [N = О]+. Аr − NН2 Аr NН − NО + Н2О;
Аr − NН2 Аr NН − NО + Н2О;

 Аr − N ≡ +NСℓ АrN ≡ +NОН¯ + КСℓ
Аr − N ≡ +NСℓ АrN ≡ +NОН¯ + КСℓ хлорид фенил диазония
хлорид фенил диазония АrN = N − ОН АrN = N − О − К + Н2О
АrN = N − ОН АrN = N − О − К + Н2О
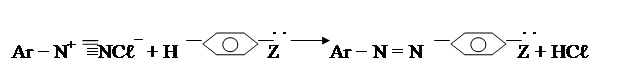 Ионы диазония являются слабыми электрофилами, и поэтому они реагируют только с ароматическими соединениями, активированными электродонорными заместителями.
Ионы диазония являются слабыми электрофилами, и поэтому они реагируют только с ароматическими соединениями, активированными электродонорными заместителями.


