Кинетически контролируемые реакции
Стартуем с главного уравнения ТАК (10.1). Рассмотрим случай бимолекулярной реакции Основное уравнение ТАК: А + B Û X ® продукты.
По физическому смыслу объем активации есть разность парциальных мольных объемов комплекса и реагентов:
Что есть объем активации? (обычно вторым членом пренебрегают ввиду малости). Экспериментально
Если у нас неполярный АК образовался из неполярных частиц, то основной вклад дает Если АК полярный и существенно отличается по полярности от исходных реагентов, то основной вклад дает 1) Пусть АК – неполярный. Если реакция мономолекулярная, то образование АК сопровождается удлинением разрываемой связи. Соответственно Бимолекулярная реакция – образуются новые связи, размеры АК меньше суммы размеров реагентов, соответственно А что насчет
Рассмотрим теперь гетеролитические реакции (влияние Сольволиз tr-BuCl в 80% СН3ОН (SN1 - механизм) (CH3)3C-Cl ¾k® (CH3)3C+ + Cl- (CH3)3C+ + Cl- + CH3OH ¾® (CH3)3COH + CH3Cl Реакция мономолекулярная, Так как фактически В случае диполя: Вывод (11.2)
В рамках данной модели при учете только сольватации диполя и в пренебрежении изменения размеров частиц от давления можно получить:
Для реакции: (C2H5)3N + (C2H5)I ® (C2H5)3Nd+…(C2H5)…Id- ® (C2H5)4N+ + I- расчет по формуле (11.3) дает
|

 , где
, где  - объем активации.
- объем активации. парциальный мольный объем реагента А [ см3/моль ].
парциальный мольный объем реагента А [ см3/моль ].  - изотермическая сжимаемость растворителя. Итого:
- изотермическая сжимаемость растворителя. Итого: (11.1)
(11.1) , где:
, где: - изменение парциальных мольных объемов частиц
- изменение парциальных мольных объемов частиц - изменение парциального мольного объема растворителя
- изменение парциального мольного объема растворителя - изменение собственного объема растворителя за счет сольватации АК (в сольватной оболочке молекулы упакованы более плотно).
- изменение собственного объема растворителя за счет сольватации АК (в сольватной оболочке молекулы упакованы более плотно).
 = -17 см3/моль при 1 атм. Объяснение – полярность переходного состояния (CH3)3Cd+¾Cld-, d ~ 0.7 – 0.9.
= -17 см3/моль при 1 атм. Объяснение – полярность переходного состояния (CH3)3Cd+¾Cld-, d ~ 0.7 – 0.9. ), то мы можем применить теоретический подход к оценке
), то мы можем применить теоретический подход к оценке  , для иона
, для иона  ,
, 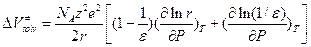
 (11.2)
(11.2)
 (11.3)
(11.3) = 7.8 Дб, что близко к экспериментальному значению, полученному при изучении зависимости ln k от e.
= 7.8 Дб, что близко к экспериментальному значению, полученному при изучении зависимости ln k от e.


