Образование химических связей
При сближении взаимодействующих атомов, например, атомов водорода, происходит перекрывание электронных облаков этих атомов. В результате перекрывания возрастает плотность отрицательного заряда в пространстве между ядрами атомов. Положительно заряженные ядра атомов притягиваются к отрицательно заряженной области перекрывания, что приводит к образованию устойчивой молекулы H2 (рисунок 1.4). Образование химической связи возможно лишь в том случае, если спины взаимодействующих неспаренных электронов противоположно направлены.
Рисунок 1.4 – Возникновение общей электронной пары при взаимодействии атомов водорода и образовании молекулы H2
Схематически образование ковалентной связи на примере образования молекул водорода, хлороводорода и азота можно показать следующим образом:
В этих схемах внешние электроны атомов обозначают точками вокруг химического символа атома; общие для двух атомов электронные пары в образовавшейся молекуле показывают точками между символами атомов. При записи графических (структурных) формул химическую связь обозначают чёрточкой, которая заменяет обозначение общей электронной пары:
Химическая связь, образованная общей для двух атомов парой электронов, называется ковалентной связью. Валентность – это число химических связей, образуемых атомом данного элемента. Выше рассмотрены примеры, в которых ковалентная связь образуется в результате взаимодействия неспаренных электронов, изначально принадлежавших двум различным атомам, и образования общей электронной пары. Такой механизм образования ковалентной связи называется обменным. Именно по обменному механизму образованы химические связи в молекулах водорода, хлороводорода и азота. Кроме обменного механизма существует донорно-акцепторный механизм образования ковалентной связи, сущность которого можно показать на примере образования иона аммония. Атом азота в молекуле аммиака связан с тремя атомами водорода тремя ковалентными связями, образованными по обменному механизму (крестиками в формуле аммиака показаны электроны, изначально принадлежавшие атомам водорода). Кроме того, у атома азота есть два спаренных электрона (неподелённая электронная пара). Такая пара электронов тоже может участвовать в образовании ковалентной связи с другим атомом, если во внешнем электронном слое этого атома
Именно по донорно-акцепторному механизму образованы ковалентные связи в комплексных ионах (см. раздел 3.1 «Понятие о комплексных соединениях»). В задании № 1 студентам предлагается записать сокращённые электронные формулы и электронно-графические схемы атомов заданных элементов в основном и возбуждённом состояниях (если возбуждённое состояние может быть реализовано в химическом процессе), а также кратко охарактеризовать биологическую роль данного элемента в живых организмах.
Пример 1.1 Запишите сокращённые электронно-графическую схему и электронную формулу атома азота в основном состоянии, проанализируйте возможность существования возбуждённых состояний и валентные возможности атома азота, охарактеризуйте биологическую роль азота в живых организмах.
Сокращённая электронная формула атома азота в основном состоянии: 2s22p3. Поскольку на втором энергетическом уровне отсутствуют d-орбитали, то возбуждённое состояние атома азота не может быть реализовано. Поэтому атом азота может образовать за счёт трёх неспаренных электронов 3 ковалентные связи по обменному механизму и 1 связь по донорно-акцепторному механизму за счёт неподелённой электронной пары. Таким образом, максимальная валентность атома азота равна 4. Азот – важнейший биогенный элемент, необходимый для существования животных и растений, он входит в состав аминокислот, важнейших биополимеров: белков, нуклеиновых кислот (ДНК, РНК), а также, витаминов, гормонов (например, адреналин, тироксин), нуклеопротеидов, хлорофилла, гемоглобина.
Пример 1.2 Запишите сокращённые электронно-графическую схему и электронную формулу атома ниобия в основном состоянии, проанализируйте возможность существования возбуждённых состояний и валентные возможности атома ниобия, охарактеризуйте биологическую роль ниобия.
Ниобий – d-элемент; у d-элементов валентными электронами являются электроны внешнего энергетического уровня и d-предвнешнего подуровня. Поскольку ниобий элемент пятого периода, то сокращённая электронная формула должна отражать строение внешнего (пятого) энергетического уровня и
Сокращённая электронная формула атома ниобия в возбуждённом состоянии Nb* – 4d35s15p1. Как видно из электронно-графической схемы атома ниобия в возбуждённом состоянии, максимальная валентность атома ниобия равна 5. Ниобий является неотъемлемым микроэлементом человеческого организма. Он концентрируется в костях, печени, мышцах, крови. Биологическая роль ниобия малоизучена. Известно, что ниобий гипоаллергенен: его можно безопасно использовать для введения в тело, так как он не вызывает биологического отторжения организмом. Это ценное свойство ниобия используется в восстановительной хирургии.
|




 ест
ест  ь свободная орбиталь. Незаполненная орбиталь есть у иона водорода, который вообще лишён электронов. При взаимодействии молекулы аммиака с ионом водорода ковалентная связь возникает вследствие того, что неподелённая пара электронов атома азота занимает свободную орбиталь иона H+ и становится общей для обоих атомов. В результате этого взаимодействия образуется ион аммония (NH4+):
ь свободная орбиталь. Незаполненная орбиталь есть у иона водорода, который вообще лишён электронов. При взаимодействии молекулы аммиака с ионом водорода ковалентная связь возникает вследствие того, что неподелённая пара электронов атома азота занимает свободную орбиталь иона H+ и становится общей для обоих атомов. В результате этого взаимодействия образуется ион аммония (NH4+):

 Азот – p-элемент; у p-элементов валентными электронами (т.е. электронами, участвующими в образовании химических связей) являются электроны внешнего энергетического уровня, поэтому сокращённая электронная формула должна отражать строение внешнего энергетического уровня атома азота. Т.к. азот – элемент второго периода, то внешние электроны располагаются на втором энергетическом уровне, который образован одной s- и тремя p-орбиталями. Азот – p-элемент пятой группы, поэтому число электронов на внешнем уровне равно 5, из которых два располагаются на более низкой по энергии 2s-орбитали и ещё 3 – на p-орбиталях.
Азот – p-элемент; у p-элементов валентными электронами (т.е. электронами, участвующими в образовании химических связей) являются электроны внешнего энергетического уровня, поэтому сокращённая электронная формула должна отражать строение внешнего энергетического уровня атома азота. Т.к. азот – элемент второго периода, то внешние электроны располагаются на втором энергетическом уровне, который образован одной s- и тремя p-орбиталями. Азот – p-элемент пятой группы, поэтому число электронов на внешнем уровне равно 5, из которых два располагаются на более низкой по энергии 2s-орбитали и ещё 3 – на p-орбиталях.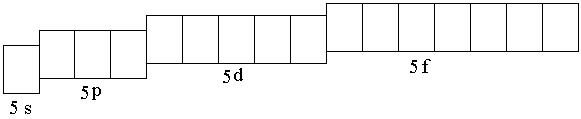

 В атоме любого d-элемента в невозбуждённом состоянии из всех орбиталей внешнего энергетического уровня занята только s-орбиталь, поэтому остальные орбитали при записи сокращённой электронно-графической схемы можно не указывать. Таким образом, валентные электроны в атоме ниобия будут располагаться на 5s-орбитали внешнего уровня и 4d-орбиталях предвнешнего. На s-орбиталях внешнего уровня у атомов
В атоме любого d-элемента в невозбуждённом состоянии из всех орбиталей внешнего энергетического уровня занята только s-орбиталь, поэтому остальные орбитали при записи сокращённой электронно-графической схемы можно не указывать. Таким образом, валентные электроны в атоме ниобия будут располагаться на 5s-орбитали внешнего уровня и 4d-орбиталях предвнешнего. На s-орбиталях внешнего уровня у атомов 



