Ідеальний газ. Дослідні закони ідеального газу
У молекулярно-кінетичній теорії користуються моделлю ідеального газу, яка відповідає таким умовам: · власний об’єм молекул газу нехтовно малий порівняно з об’ємом посудини; · між молекулами газу відсутні сили взаємодії; · зіткнення молекул газу між собою і стінками посудини абсолютно пружні. Модель ідеального газу можна використовувати при вивченні реальних газів, оскільки вони за умов, близьких до нормальних (Р = Р А, Т = 273 К), а також при низьких тисках і високих температурах близькі за своїми властивостями до ідеального газу. Розглянемо деякі термодинамічні ізопроцеси, у яких відбувається зміна термодинамічних параметрів, що визначають стан газу. Ізопроцесом називається процес, у якому один з параметрів стану (P, V або T) залишається постійним, а інші змінюються. Процес, який протікає у газі, коли температура залишається постійною (Т = const), називається ізотермічним процесом. Для такого процесу виконується закон Бойля-Маріотта: для даної маси газу (т = const) при постійній температурі добуток тиску газу на його об'єм є величиною постійною: PV = const, або Тобто при постійній температурі тиск газу зменшується обернено пропорційно зростанню температури. Діаграма цього ізопроцесу в координатах P-V є гіперболою (рис. 2.1). Процес, який протікає у газі, коли об’єм залишається постійним (V = const), називається ізохорним процесом. Для такого процесу виконується закон Шарля: для даної маси газу (т = const) при постійному об’ємі відношення тиску газу до його температури є величиною постійною:
Тобто тиск газу, який знаходиться у замкнутому об’ємі, зростає прямо пропорційно зростанню термодинамічної температури. Діаграма цього ізопроцесу у координатах P-T є прямою лінією (рис. 2.2). Процес, який протікає у газі, коли тиск залишається постійним (Р = const), називається ізобарним процесом. Для такого процесу виконується закон Гей-люсака: для даної маси газу (т = const) при постійному тиску відношення об’єму газу до його температури є величиною постійною:
Тобто об’єм газу при постійному тиску зростає прямо пропорційно зростанню термодинамічної температури. Діаграма цього ізопроцесу у координатах V-T є прямою лінією (рис. 2.3). Закон Авогадро: молі будь-яких газів при однакових температурі й тиску займають однакові об’єми. За нормальних умов (P = PА = 1,03×105 Па, Закон Дальтона: тиск суміші ідеальних газів дорівнює сумі парціальних тисків газів, з яких вона складається:
Парціальний тиск – це тиск газу, який входить до суміші, в об’ємі цієї суміші.
Рівняння Менделєєва- Клапейрона Наслідком дослідних законів ідеального газу є рівняння Клапейрона, яке виконується для даної маси газу (т = const):
|

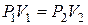 .
.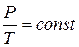 , або
, або 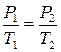 .
.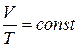 , або
, або 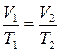 .
.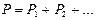 .
.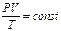 або
або 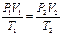 .
.


