– Задача. Определить активность и коэффициент активности кислорода в расплавах Fе–О по данным о химическом равновесии расплава с паро-водородной смесью:
Н2 (г) + [О] = Н2O(г). (1.21)
– Исходные данные. Расплав железа, содержащий кислород, приводится в равновесие с паро-водородной смесью. Отношения  в зависимости от концентрации растворенного в железе кислорода и температуры приведены в таблице (по данным В.В. Аверина).
в зависимости от концентрации растворенного в железе кислорода и температуры приведены в таблице (по данным В.В. Аверина).
– Звездочкой отмечены насыщенные растворы кислорода в железе (на поверхности металлического расплава образуется пленочка FеО).
– Теория. Константа равновесия реакции (1.21)
 . (1.22)
. (1.22)
Зависимость отношения 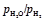 от концентрации и температуры
от концентрации и температуры
| [% O]
| p H2O/ p H2
| [% O]
| p H2O/ p H2
| [% O]
| p H2O/ p H2
| [% O]
| p H2O/ p H2
|
| T = 1824 K
| T = 1847 K
| T = 1870 K
| T = 1894 K
|
| 0,0305
| 0,135
| 0.0344
| 0.132
| 0.0420
| 0.132
| 0.0451
| 0.132
|
| 0,0412
| 0,184
| 0.0385
| 0.132
| 0.0438
| 0.132
| 0.0630
| 0.185
|
| 0,1031
| 0,434
| 0.0464
| 0.184
| 0.0565
| 0.185
| 0.0647
| 0.185
|
| 0,1405
| 0,544
| 0.0898
| 0.322
| 0.1040
| 0.322
| 0.1187
| 0.322
|
| 0,1520
| 0,598
| 0.0887
| 0.322
| 0.1047
| 0.322
| 0.1140
| 0.322
|
| 0,1711
| 0,651
| 0.1570
| 0.540
| 0.1444
| 0.426
| 0.1593
| 0.426
|
|
|
| 0.1600
| 0.540
| 0.1763
| 0.540
| 0.2100
| 0.540
|
|
|
| 0.1697
| 0.598
| 0.1787
| 0.540
| 0.2112
| 0.540
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
– Для расчета активности кислорода должны быть известны отношения  и значения K. Константа равновесия химической реакции зависит только от температуры. Если в качестве стандартного состояния принять разбавленный идеальный 1 %-ный раствор [О], то величину K можно определить по данным в области разбавленных растворов, где f [O] = 1 и a [O] = [% О]. Для этих растворов
и значения K. Константа равновесия химической реакции зависит только от температуры. Если в качестве стандартного состояния принять разбавленный идеальный 1 %-ный раствор [О], то величину K можно определить по данным в области разбавленных растворов, где f [O] = 1 и a [O] = [% О]. Для этих растворов
 . (1.23)
. (1.23)
– Комбинируя уравнения (1.22) и (1.23), определяем активность и коэффициент активности кислорода.
– Решение. Для определения константы равновесия реакции (1.21) строим зависимости отношения  от концентрации растворенного в железе кислорода. Экстраполяцией экспериментальных кривых к точке [ % О] = 0 находим значения K, равные при температурах 1824, 1847, 1870, 1894 К соответственно 4,395; 3,705; 3,220 и 2,805. Активность кислорода в зависимости от состава и температуры вычисляем по уравнению (1.22). Например, при [% О] = 0,1405 и
от концентрации растворенного в железе кислорода. Экстраполяцией экспериментальных кривых к точке [ % О] = 0 находим значения K, равные при температурах 1824, 1847, 1870, 1894 К соответственно 4,395; 3,705; 3,220 и 2,805. Активность кислорода в зависимости от состава и температуры вычисляем по уравнению (1.22). Например, при [% О] = 0,1405 и
Т = 1824 К  = 0,544 (см. исходные данные), K = 4,395
= 0,544 (см. исходные данные), K = 4,395
 = 0,544/4,395 = 0,124.
= 0,544/4,395 = 0,124.
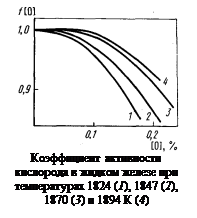
– Отсюда f [O] = a [O]/[% O] = 0,124/0,1405 = 0,881. Результаты расчета f [O] приведены на рисунке.
–
 Примечания
Примечания. 1. Растворы кислорода в жидком железе характеризуются слабыми отрицательными отклонениями от закона Генри (
f [O] < 1).
– 2. Отклонения от закона Генри уменьшаются с повышением температуры; по мере повышения температуры раствор приближается к идеальному разбавленному раствору (f [O] ® 1).
– Просуммировав реакцию (1.21) с реакцией образования водяного пара (H2(г) +  O2(г) = H2O(г)), можно определить термодинамические свойства процесса растворения газообразного кислорода в жидком железе (
O2(г) = H2O(г)), можно определить термодинамические свойства процесса растворения газообразного кислорода в жидком железе ( O2(г) = [O]).
O2(г) = [O]).
 Примечания. 1. Растворы кислорода в жидком железе характеризуются слабыми отрицательными отклонениями от закона Генри (f [O] < 1).
Примечания. 1. Растворы кислорода в жидком железе характеризуются слабыми отрицательными отклонениями от закона Генри (f [O] < 1).

 в зависимости от концентрации растворенного в железе кислорода и температуры приведены в таблице (по данным В.В. Аверина).
в зависимости от концентрации растворенного в железе кислорода и температуры приведены в таблице (по данным В.В. Аверина). . (1.22)
. (1.22)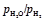 от концентрации и температуры
от концентрации и температуры . (1.23)
. (1.23) = 0,544/4,395 = 0,124.
= 0,544/4,395 = 0,124. O2(г) = H2O(г)), можно определить термодинамические свойства процесса растворения газообразного кислорода в жидком железе (
O2(г) = H2O(г)), можно определить термодинамические свойства процесса растворения газообразного кислорода в жидком железе (


