Активность углерода в расплавах Fe–C
– Задача. Определить активность углерода в расплавах Fe–C при 1883 К по данным о химическом равновесии [C] + CO2 (г) = 2CO(г). (1.19) – Исходные данные. 1. Расплав Fe–C находится в равновесии с газовой смесью CO2 и CO. Отношения
– 2. Константа равновесия реакции C(гр) + CO2 (г) = 2СО(г) (1.20) – определяется по формуле lg K ¢ = (-8407/ T) + 8,76. – Теория. Формула для определения константы равновесия реакции (1.19) имеет вид: K = – Если в качестве стандартного состояния для растворенного углерода выбрать графит, то K = K', где K' - константа равновесия реакции (1.20). Тогда
– Решение. Вычислим активность углерода в расплаве, содержащем 0,49 % С. При 1833 К lg K' = -(8407/1833) + 8,76 = 4,17; K' = 1,48×104. – Константа равновесия K' определена для давления, выраженного в атмосферах. Следовательно, давление должно быть выражено в атмосферах (1 атм = 1,01×105 Па). – Получим K' = 1,48×104×1,01×105 = 1,49×109. Тогда a С = – Рассчитанная таким образом активность углерода в расплавах Fе–С в зависимости от [% С]:
– Примечание. Приведенные исходные данные позволяют определить активность углерода и для стандартного состояния по Генри. Необходимую для этого константу равновесия реакции [С]1 % +
|

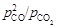 в зависимости от концентрации углерода при 1883 К по данным Ричардсона и Дениса приведены ниже:
в зависимости от концентрации углерода при 1883 К по данным Ричардсона и Дениса приведены ниже: P2CO/PCO2, МПа
P2CO/PCO2, МПа
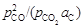 .
.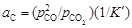 .
. = (29,9×106)/(1,49×109) = 0,026.
= (29,9×106)/(1,49×109) = 0,026.


