Дослiд 9.3. Окислення етилового спирту перманганатом калiю
У суху пробiрку вносять 2 краплi етилового спирту, 2 краплi розчину перман-ганату калiю i 3 краплi розчину сiрчаної кислоти. Обережно нагрiвають вмiст пробiрки над полум’ям пальника. Рожевий розчин знебарвлюється. Вiдчувається характерний запах оцтового альдегiду. В чисту пробiрку вносять 3 краплi фуксинсiрчистої кислоти i краплю знебарвленого розчину - поступово з’являється рожевий колiр.
Хiмiзм процесу: KMnO4 + H2SO4 ® HMnO4 + KHSO4; марганцева кислота 2HMnO4 ® Mn2O7 + H2O Mn2O7 ® 2MnO + 5“O” CH3 - CH2OH + ”O” ® MnO + H2SO4 ® MnSO4 + H2O 2KMnO4 + 5C2H5OH + 2H2SO4 Спирти окислюються краще, нiж вiдповiднi їм насиченi вуглеводнi, що поясню-ється впливом гiдроксильної групи, присутньої в молекулi. Первиннi спирти при окис-леннi в м’яких умовах перетворюються в альдегiди, а в жорстких - утворюють кис-лоти.
|

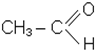 + H2O
+ H2O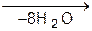 5
5 


