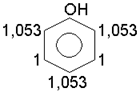
Будова, iзомерiя, номенклатура i властивостi. Органiчнi сполуки, в яких гiдроксил приєднується до атома вуглецю ароматич-ного ядра, називаються фенолами.
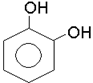
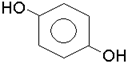
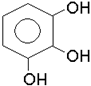
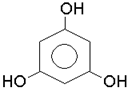
Органiчнi сполуки, в яких гiдроксил приєднується до атома вуглецю ароматич-ного ядра, називаються фенолами. За кiлькiстю гiдроксильних груп феноли дiляться на одно- i багатоатомнi, наприклад:
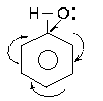
Властивостi фенолiв пояснюються їх електронною будовою:
Неподiлена електронна пара атомiв кисню перебуває у сполученнi з p-елек-тронами бензольного ядра i притягується до ядра. Це зменшує електронну густину бiля атома кисню i вiн слабше, нiж у спиртах, притягує атом водню. Виникає значно бiльша, нiж у спиртiв, можливiсть дисоцiацiї у фенолiв зв’язку О-Н з вiдщепленням протона, i у водних розчинах феноли поводяться як слабкi кислоти: C6H5OH 2C6H5OH + 2Na ® 2C6H5ONa + H2 На вiдмiну вiд спиртiв феноли можуть утворювати феноляти i при дiї водних розчинiв лугiв: C6H5OH + NaOH ® C6H5ONa + H2O Проте феноли - дуже слабкi кислоти: вони не забарвлюють лакмус у червоний колiр, солетворнi похiднi їх - феноляти - у водних розчинах сильно гiдролiзованi i навiть такi слабкi кислоти, як вугiльна, витісняють iз фенолятiв вiльнi феноли: C6H5ONa + CO2 + H2O ® C6H5OH + NaHCO3 Такий вплив ароматичного ядра на гiдроксильну групу. Але i гiдроксильна група, в свою чергу, впливає на властивостi ароматичного ядра. Внаслiдок супря-ження p-електронної системи бензольного ядра з неподiленими електронами атома кисню збiльшується його активнiсть в електрофiльних реакцiях. Розрахована елект-ронна густина на атомах вуглецю в молекулi фенолу:
Гiдроксильна група у фенолах - сильний орто-пара-орiєнтант; вона значно полегшує реакцiї в бензольному ядрi, зокрема сульфування, нiтрування, галоге-нування.
|




 C6H5O- + H+
C6H5O- + H+