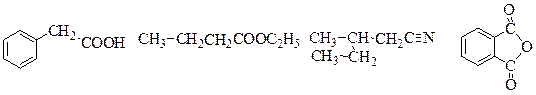ЛАБОРАТОРНАЯ РАБОТА №6
Опыт 1. Выделение жирных кислот из мыла и получение кальциевых солей. Получите у лаборанта 10 мл раствора мыла в воде. Раствор разлейте в две пробирки по 5 мл. а) В первую пробирку с раствором мыла добавьте 2 мл разбавленной серной кислоты. Происходит обменная реакция и выделяется жирная кислота, которая в воде не растворяется. Поэтому раствор становится мутным. Нагрейте полученную смесь, а затем охладите. При нагревании жирные кислоты всплывают наверх, а при охлаждении они затвердевают. Наблюдения и выводы запишите в журнал. б) Во вторую пробирку с раствором прибавьте 2 мл раствора хлористого кальция. Энергично взболтайте. Образуется осадок кальциевых солей высших жирных кислот. Эти соли не растворяются в воде. Наблюдения и выводы запишите в журнал.
Опыт 2. Получение эфиров жирных кислот. Получение этилацетата и изоамилацетата. а) Уксусноэтиловый эфир (этилацетат). Внесите в пробирку 2 мл этилового спирта, 2 мл ледяной уксусной кислоты и 1 мл концентрированной серной кислоты. Смесь хорошо перемешайте стеклянной палочкой и нагревайте 2 минуты на водяной бане. В результате реакции этерификации образуется уксусноэтиловый эфир, обладающий приятным запахом. Наблюдения и выводы запишите в журнал. б) Уксусноизоамиловый эфир (изоамилацетат) внесите в пробирку 2 мл изоамилового спирта (3-метилбутанол-1), 2 мл ледяной уксусной кислоты и 0,5 мл концентрированной серной кислоты. Смесь перемешайте и нагревайте 5 минут на водяной бане. Наблюдения и выводы запишите в журнал. Содержимое пробирки охладите и вылейте в другую пробирку с водой. Эфир всплывет наверх. Уксусноизоамиловый эфир имеет запах грушевой эссенции.
Опыт 3. Непредельные кислоты. Свойства олеиновой кислоты. а) Получение соли олеиновой кислоты. Налейте в пробирку 1 мл олеиновой кислоты и добавьте 2 мл воды. Обратите внимание на растворимость олеиновой кислоты в воде. Добавьте 2 мл концентрированной щелочи (NaOH); встряхните смесь. Наблюдения и выводы запишите в журнал. б) Реакция олеиновой кислоты с бромной водой. К 1 мл олеиновой кислоты прибавьте 1 мл бромной воды и сильно встряхните. Бромная вода обесцвечивается, так как бром присоединяется по двойной связи олеиновой кислоты. в) Окисление олеиновой кислоты. К 1 мл олеиновой кислоты прибавьте 2 мл раствора марганцовокислого калия. Энергично перемешайте содержимое пробирки. Олеиновая кислота окисляется до диоксистеариновой кислоты, а марганцовокислый калий восстанавливается с выделением двуокиси марганца. Наблюдения и выводы запишите в журнал.
Опыт 4. Двухосновные кислоты. Получение кислых и средних солей щавелевой и винной кислот. а) Соли щавелевой кислоты. К 2 мл 2н. раствора щавелевой кислоты прибавьте 1 мл 2н. раствора едкого калия. Образуется осадок труднорастворимого кислого щавелевокислого калия. При дальнейшем добавлении щелочи осадок растворяется с образованием средней калиевой соли щавелевой кислоты. Наблюдения и выводы запишите в журнал. б) Соли винной кислоты. Налейте в пробирку 2 мл 1н. раствора винной кислоты и прибавьте 1 мл 1н. раствора едкого калия. Выпадает осадок кислой калиевой соли винной кислоты. При дальнейшем добавлении щелочи образуется средняя калиевая соль винной кислоты, которая хорошо растворяется в воде. Наблюдения и выводы запишите в журнал.
Задачи (карбоновые кислоты) 1. Приведите структурные формулы следующих кислот: терефталевой, изомасляной, метакриловой, малоновой, олеиновой, g-циановалериановой, 2,3-диметилпентановой, глутаровой, малеиновой. 2. Назовите соединения по номенклатуре IUPAC:
3. Напишите реакции получения соответствующих кислот из: 1,1,1-трибромпропана, бензилового спирта, глутарового альдегида, бутена-2, бромистого этила. 4. Приведите уравнения реакций между следующими соединениями: хлорангидридом масляной кислоты и метиламином, уксусной кислотой и пентоксидом фосфора, метанолом и пропионовой кислотой (H+), пропановой кислотой и трихлоридом фосфора, 2-метилбутановой кислотой и бромом (hn). 5. Какие продукты образуются при взаимодействии бензойной кислоты с аммиаком (сильное нагревание), PCl5, СаСО3, BaO, C2H5OH/Н+, бромом (в присутствии AlCl3)? 6. Напишите соединения, которые образуются при нагревании янтарной, малоновой, метилмалоновой и щавелевой кислот. 7. Что образуется при взаимодействии акриловой кислоты с бромистым водородом, метанолом (H+), хлором, NaOH? 8. Почему малеиновая кислота способна образовывать ангидрид, а фумаровая нет? Как вы думаете, что получается при нагревании глутаровой кислоты с пентоксидом фосфора? 9. Какое соединение образуется при последовательной обработке бромбензола магнием (в абсолютном эфире), СО2, затем водой? 10. Расположите кислоты в ряд по возрастанию их кислотных свойств: а) трифторуксусная, трихлоруксусная, уксусная; б) уксусная, щавелевая, трифторуксусная; в) 2,2-диметилпропановая, пентановая, 2,2-дибромпентановая. Ответ поясните. 11. С помощью каких реакций можно различить пропионовую, акриловую и малоновую кислоты?
Задачи (оксикислоты) 1. Приведите структурные формулы молочной, салициловой, b-гидроксивалериановой, гликолевой, винной и лимонной кислот. Назовите их по номенклатуре IUPAC. 2. В чём заключается оксинитрильный синтез a-оксикислот? Какие кислоты можно получить этим методом исходя из уксусного альдегида, бутаналя, 2-бутанона? 3. Напишите три метода синтеза b-гидроксипропионовой кислоты. 4. Как взаимодействует b-гидроксимасляная кислота с содой, натрием, гидроксидом кальция, амидом натрия. Почему карбоксильная группа проявляет гораздо более кислые свойства, чем гидроксильная? 5. Напишите реакции молочной кислоты с трихлоридом фосфора, этиловым спиртом (в присутствии серной кислоты), НBr, уксусным ангидридом, этиламином (при нагревании), КMnO4 (H+). 6. Какие кислоты образуются при гидратации или гидролизе следующих соединений: 3,3,3-трибромпропилового спирта, 2-бутеновой кислоты, нитрила 4-гидроксигексановой кислоты, аспирина? 7. Приведите уравнения реакций которые протекают при нагревании a-гидроксипропионовой, b-гидрокси-a-хлорвалериановой и g-гидроксимасляной, b-окси-a-метилкапроновой кислот. 8. Определите структуру, назовите и напишите схему синтеза соединения С2Н2О3, если известно, что оно взаимодействует с этиловым спиртом (в присутствии серной кислоты), образует хлорангидрид и амид, восстанавливает Ag2O и Cu(OH)2.
|