
Головна сторінка Випадкова сторінка
КАТЕГОРІЇ:
АвтомобіліБіологіяБудівництвоВідпочинок і туризмГеографіяДім і садЕкологіяЕкономікаЕлектронікаІноземні мовиІнформатикаІншеІсторіяКультураЛітератураМатематикаМедицинаМеталлургіяМеханікаОсвітаОхорона праціПедагогікаПолітикаПравоПсихологіяРелігіяСоціологіяСпортФізикаФілософіяФінансиХімія
Державна екологічна експертиза.
Дата добавления: 2015-08-17; просмотров: 712
|
|
Измельченный растительный материал (картофель, лук, капуста, зелень и др.) в количестве 2-10 г помещают в диализационный цилиндр (стеклянную трубку с мембраной). Отмеривают 100 мл дистиллированной воды в стакан и помещают туда диализационный цилиндр с биоматериалом, предварительно смочив его несколькими миллилитрами дистиллированной воды из первоначального объема воды в стакане. Воды приливают столько, чтобы она хорошо смочила пробу. Проводят диализ в течение 1,5 - 2 часов.
Не вынимая диализационного цилиндра из стакана, пипеткой отбирают 10 мл диализата для анализа на нитриты и 5 мл для анализа на нитраты.
Количественное определение нитритов.
К 10 мл диализата, помещенного в пробирку добавляют 1 мл реактива Грисса, встряхивают содержимое пробирки. Через 15 мин. определяют оптическую плотность полученного раствора при λ = 540 нм в кюветах с толщиной поглощающего слоя 1 см. В качестве раствора сравнения используют дистиллированную воду.
Количественное определение нитратов.
К 5 мл диализата, помещенным в пробирку с притертой пробкой, в которую предварительно помещают 0,3 г сухого восстановителя, приливают 5 мл 12% уксусной кислоты, закрывают пробирку пробкой и энергично встряхивают ее в течение точно 2 мин.
В параллельную пробирку помещают 0,3 г сухого восстановителя и приливают 10 мл 12% уксусной кислоты, закрывают ее пробкой и встряхивают в течение 2 мин. ("холостой" раствор).
Через 10 мин. переливают содержимое пробирок в центрифужные пробирки и центрифугируют при 5 - 6 тыс. об./мин. в течение 5 мин. После этого определяют оптическую плотность исследуемого раствора при λ = 540 нм в кюветах с толщиной поглощающего слоя 1 см. В качестве раствора сравнения используют "холостой" раствор - раствор уксусной кислоты, обработанный сухим восстановителем.
По калибровочным графикам находят содержание нитратов (нитрат - иона) и нитритов (нитрит – иона) и рассчитывают их концентрацию в исходном биологическом материале по формуле:
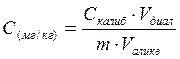 ,
,
Где: Cкалиб – концентрация нитрит-иона (нитрат-иона), найденная по калибровочному графику, мкг;
Vдиал – объем диализата, мл;
Vаликв – объем аликвоты, взятой для анализа, мл;
m – масса навески биоматериала, г.
В том случае, если в пробах устанавливается наличие большого содержания нитритов - свыше 20 мкг (интенсивная окраска в пробирке), их следует удалять, так как они несколько завышают результаты определения нитратов. Для удаления нитритов к диализату в стакане, соответственно 50 или 100 мл, прибавляют 2 - 4 мл 1-процентного раствора сульфаминовой кислоты, перемешивают раствор стеклянной палочкой и оставляют на 5 мин. После этого отбирают 5 мл диализата для анализа на нитраты и проводят анализ, как описано выше. При расчетах учитывают увеличение общего объема пробы.
Построение калибровочных кривых
1. Построение калибровочной кривой для определения нитритов.
В 11 химических пробирок помещают рабочий раствор нитрита натрия в количествах, указанных в таблице. Объем в пробирках доводят дистиллированной водой до 10 мл. Приливают по 1 мл реактива Грисса и энергично встряхивают.
Таблица: Данные для приготовления стандартных растворов для определения нитритов.
| № пробирки | Количество рабочего раствора NaNO2, мл | Содержание NO2 | |
| мг | мкг | ||
| 0,1 | 0,0005 | 0,5 | |
| 0,2 | 0,0010 | 1,0 | |
| 0,4 | 0,0020 | 2,0 | |
| 0,6 | 0,0030 | 3,0 | |
| 0,8 | 0,0040 | 4,0 | |
| 1,0 | 0,0050 | 5,0 | |
| 1,2 | 0,0060 | 6,0 | |
| 1,4 | 0,0070 | 7,0 | |
| 1,6 | 0,0080 | 8,0 | |
| 1,8 | 0,0090 | 9,0 | |
| 2,0 | 0,0100 | 10,0 |
Для построения калибровочной кривой через 15 мин. определяют оптическую плотность полученных растворов при λ = 540 нм в кюветах с толщиной слоя 1 см. В качестве раствора сравнения используют дистиллированную воду.
2. Построение калибровочной кривой для определения нитратов.
В 7 пробирок с притертыми пробками или в 7 центрифужных пробирок с притертыми пробками последовательно прибавляют по 0,3 г реактива для восстановления нитратов, затем приливают рабочий раствор и 12% уксусную кислоту в количествах, указанных в таблице (общий объем составляет 10 мл).
Таблица: Данные для приготовления стандартных растворов для определения нитратов.
| № пробирки | Количество рабочего раствора NaNO2, мл | Содержание NO2 | Кол-во 1% уксусной кислоты, мл | |
| мг | мкг | |||
| 0,0 | 0,0 | - | 10,0 | |
| 1,0 | 0,010 | 9,0 | ||
| 2,0 | 0,020 | 8,0 | ||
| 4,0 | 0,040 | 6,0 | ||
| 6,0 | 0,060 | 4,0 | ||
| 8,0 | 0,080 | 2,0 | ||
| 10,0 | 0,100 | 0,0 |
Затем пробирки или центрифужные пробирки закрывают пробками и энергично встряхивают в течение ровно 2 мин. Через 10 мин. пробы центрифугируют в центрифужных пробирках при 5 - 6 тыс. об./мин. в течение 5 мин. После этого определяют оптическую плотность исследуемого раствора при λ = 540 нм в кюветах с толщиной поглощающего слоя 1 см. В качестве раствора сравнения используют "холостой" раствор - раствор уксусной кислоты, обработанный сухим восстановителем
Вопросы для самоконтроля.
1. Каковы особенности исследования на наличие минеральных кислот в биоматериале и биожидкости?
2. Какие предварительные испытания на вещества, изолируемые настаиванием с водой, вы знаете?
3. Какие объекты следует направлять на исследования при остром отравлении минеральными кислотами?
4. Какие объекты следует направлять на исследования при остром отравлении едкими щелочами?
5. Какие существуют методы изолирования и очистки извлечений при отравлениях минеральными кислотами, едкими щелочами?
6. Как проводится химико-токсикологический анализ на наличие серной кислоты?
7. Как проводится химико-токсикологический анализ на присутствие азотной кислоты?
8. Каковы особенности проведения исследования на наличие хлористоводородной кислоты?
9. Токсикологическое значение минеральных кислот, симптомы отравления, первая помощь при отравлении ими.
10. В чем заключается особенность обнаружения аммиака в биологическом материале? Интерпретация результатов исследования на наличие аммиака.
11. Как проводится химико-токсикологический анализ на наличие натрия гидроксида?
12. Химико-токсикологический анализ на присутствие солей азотной и азотистой кислот (нитритов и нитратов).
13. Как отличить едкую щелочь от растворов карбонатов (гидрокарбонатов)?
14. Как отличить минеральные кислоты от органических?
| <== предыдущая лекция | | | следующая лекция ==> |
| Об’єкти та суб’єкти екологічної експертизи. | | | Громадська екологічна експертиза. |