Методика дистилляции с водяным паром.
Установка для проведения перегонки с водяным паром приведена на рисунке 1. Прибор состоит из четырех частей: парообразователя; круглодонной колбы, холодильника и приемника. Колбу для перегонки в процессе дистилляции нагревают на водяной бане.
Рис. 1. Установка для изолирования летучих ядов перегонкой с водяным паром. 1 - парообразователь; 2 – колба с объектом исследования; 3 - холодильник; 4 – приемник дистиллята, 5 – водяная баня.
Парообразователь представляет собой сосуд с отводной боковой трубкой, которая служит для соединения его с колбой. Для уравновешивания давления в горлышко парообразователя вставляется длинная стеклянная трубка (~1 м), доходящая почти до дна цилиндра. Парообразователь заполняют водой на 1/3 – 1/4 объема. О количестве введенной в него воды судят по водомерной трубке. Биологический материал смешивают с дистиллированной водой до густоты кашицы и помещают в круглодонную колбу с таким расчетом, чтобы колба была заполнена не более чем на 1/3 ее объема. Колбу с объектом закрепляют в штативе, глубоко погружают в холодную водяную баню и закрывают пробкой так, чтобы конец стеклянной трубки, вводящей пар, доходил почти до дна колбы. Когда прибор подготовлен, парообразователь нагревают. После того как в парообразователе пойдет пар, объект подкисляют виннокаменной или щавелевой кислотой до pH=2. После этого соединяют все части прибора и доводят водяную баню до кипения, чтобы уменьшить конденсацию водяного пара в колбе. Дистилляция производится по возможности медленно, так, чтобы можно было считать капли в приемнике. Это достигается регулированием нагревания парообразователя. В зависимости от исследуемого токсиканта приёмник должен быть охлажден. После окончания дистилляции сначала отсоединяют от парообразователя колбу с биоматериалом, потом прекращают нагревать парообразователь и водяную баню. В процессе исследования дистилляты хранят в закрытых пробками колбах. При необходимости проведения количественного определения того или иного вещества отгонку дистиллята ведут до полного его изолирования из биологического материала, что узнается по получению отрицательного результата качественных реакций на это вещество (при исследовании последней порции дистиллята). При перегонке с водяным паром из подкисленного объекта первые порции дистиллята собирают в объеме 3 мл в заранее подготовленную коническую колбу-приемник с 2 мл 5% раствора гидроксида натрия во избежание потерь синильной кислоты (при количественном определении – в титрованный раствор нитрата серебра), для чего конец трубки вводят в приемник таким образом, чтобы он был погружен в щелочь, находящуюся в нем. Второй и третий дистилляты собирают в приемники без едкой щелочи в количестве 25 мл каждый. При отсутствии синильной кислоты данную операцию исключают. При специальном исследовании на метанол приемник охлаждают льдом для уменьшения потерь искомого токсического вещества. При целенаправленном исследовании на этанол приемник охлаждают водой, чтобы предотвратить испарение спирта. Ввиду высокой летучести уксусной кислоты при перегонке ее собирают в сосуд, содержащий 0,1 М раствор едкого натра. При изолировании с водяным паром веществ основного характера из подщелоченного объекта, дистиллят собирают в раствор кислоты хлористоводородной.
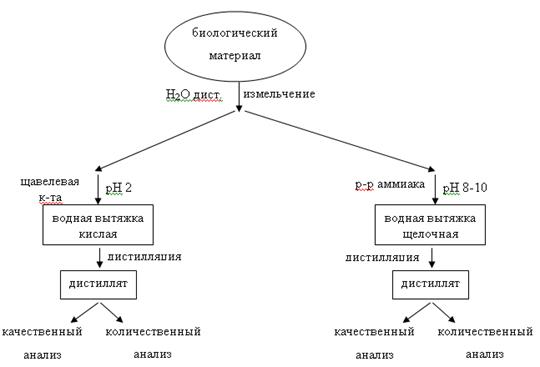
Рис. 2. Схема изолирования из биологического материала.
Подкисление биологического материала до рН 2 - 3 необходимо для достижения максимальной степени изолирования токсических веществ. При этом значении рН (оно является изоэлектрической точкой белка) происходит разрушение комплекса токсичного вещества с белковыми структурами биотканей. Подкисление или подщелачивание биологического материала зависит от характера соединения. Выделение соединений обладающих кислотными свойствами требует кислой реакции среды, соединений обладающих основными свойствами – щелочных или слабокислых сред, соединений обладающих нейтральными свойствами – кислых или щелочных сред. Подкисление биологических объектов может осуществляться как слабыми органическими кислотами, так и сильными минеральными кислотами. Слабые органические кислоты (щавелевая и винная) используются в случае предотвращения разложения лабильных соединений, которые естественным путем образуются в организме (конъюгаты фенолов с серной или глюкуроновой кислотами) или попадающих извне (при отравлении синильной кислотой и ее солями). Использование сильных минеральных кислот необходимо для предотвращения диссоциации определяемого вещества и перевода его в молекулярную форму, с целью полноты извлечения. Так при перегонке с водяным паром уксусной кислоты используются фосфорная или серная кислоты. Они предотвращают ее диссоциацию в водной среде (рКа уксусной кислоты - 4,74; серной кислоты - -3; фосфорной кислоты – 1,8). Применение минеральных кислот обусловлено необходимостью разрушения конъюгатов, образующихся между токсичными веществами, продуктами их метаболизма и эндогенными кислотами.
К достоинствам метода перегонки с водяным паром относятся: ü при изолировании происходит одновременная очистка анализируемых веществ; ü возможность изолирования веществ, которые имеют высокую температуру кипения, разлагаются при температуре кипения, нерастворимы в воде; ü возможность извлекать вещества различных химических классов. Недостатки метода: длительность, трудоемкость и наличие специальной литературы. Кроме перегонки с водяным паром для извлечения токсичного соединения из биологического объекта используют методы микроперегонки и микродистилляции. Микроперегонка. Метод основан на ускоренной диффузии «летучих» веществ из биологической пробы при повышенной температуре в присутствии сильных электролитов и проводится в герметически закрытом флаконе. Парогазовая фаза отбирается микрошприцом и используется для анализа. Микродиффузия. Метод основан на переходе в закрытой камере через газовую фазу молекул летучего вещества из камеры с высоким его содержанием (жидкая фаза 1) в камеру с низким его содержанием (жидкая фаза 2). В соответствии с законом Рауля процесс будет продолжаться до выравнивания концентраций в жидких фазах. При этом давление пара над обеими камерами станет одинаковым. Каждая камера заполняется соответствующим вытесняющим (жидкость 1) и абсорбирующим агентом (жидкость 2). Методом микродиффузии можно изолировать ацетальдегид, ацетон, метанол, изопропанол, фенол, толуол и др. Также существуют методы фракционной перегонки, паровоздушной дистилляции, суховоздушной дистилляции, прямой экстракции органическим растворителем. При проведении исследования на группу «летучих» ядов, необходимо обращать внимание на следующее: Запах объекта (иногда это может дать какие-либо дополнительные ориентирующие данные). Однако следует учитывать, что запах биологического объекта, как правило, маскирует запах летучего ядовитого вещества, но в некоторых случаях все же возможно определение запаха искомого соединения. Например, изоамиловый спирт придает объекту запах сивушных масел, нитробензол и синильная кислота - запах горького миндаля. Запах и внешний вид дистиллята. Перед выполнением химического исследования обязательно проводят наружный осмотр дистиллята, обращая внимание на его прозрачность или мутность, наличие капель на дне склянки или маслянистой пленки на поверхности жидкости, наличие характерного запаха. Характеристика и анализ веществ группы «Летучие яды»
|