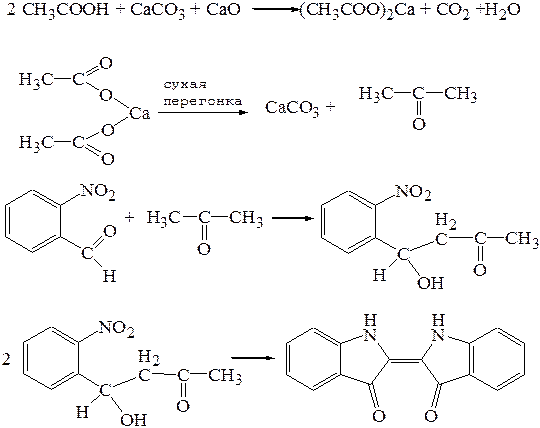Токсикологическое значение и метаболизм.
Отравления уксусной кислотой достаточно часты, что обусловлено ее доступностью. Большая часть отравлений уксусной кислотой носит суицидальный характер. Смертельная доза ледяной уксусной кислоты – 12 – 15 г, уксусной эссенции – 20 – 40 мл (10 – 20 г); столового уксуса – около 200 мл. Поступление в организм уксусная кислота происходит в основном перорально, ингаляционно и через кожные покровы. При местном контакте с кожей уксусная кислота с концентрацией более 30% способна вызывать ожоги и образование струпов. Местное действие уксусной кислоты слабее, чем у неорганических кислот. Вдыхание паров уксусной кислоты приводит к раздражению слизистых оболочек верхних дыхательных путей, появлению кашля, затруднению дыхания, появлению болей в груди, тошноты, рвоты. Происходит развитие бронхопневмоний и воспаление глотки. Причиной смерти является асфиксия и тяжелые поражения легких. Пероральное отравление уксусной кислотой характеризуется резкими болями в ротовой полости и по ходу пищеварительного тракта. Появляются ожоги слизистых ротовой полости, глотки, пищевода, желудка и кишечника, сопровождающиеся «кровавой» рвотой. Рвотные массы обладают характерным запахом. Резорбтивное действие уксусной кислоты проявляется кислотным гемолизом (уксусная кислота относиться к гемолитическим ядам). Гемолиз сопровождается гемоглобинурией (выделение растворенного гемоглобина почками). Моча приобретает темно-красный цвет и содержит белок, развивается острая почечная недостаточность. Нарушения со стороны ЦНС вызваны появлением возбуждения, слуховыми и зрительными галлюцинациями. При паталогоанатомическом вскрытии наблюдаются ожоги слизистых ЖКТ, иногда перфорация стенок пищевода и желудка, острая дистрофия печени, нефроз, пневмония. В организме уксусная кислота метаболизируется до ацетальдегида, превращающегося частично в этиловый спирт и частично разлагающегося с образованием CO2 и воды. Выводиться из организма через легкие, с мочой и калом, как в неизменном виде, так и в виде метаболитов. Следует отметить, что уксусная кислота является естественной составной частью организма человека, в обычных условиях присутствует в ряде внутренних органов и в небольших количествах выделяется с мочой и калом. При приёме уксусной кислоты внутрь следует выпить большое количество жидкости. Вызов рвоты является крайне опасным, так как вторичное прохождение кислоты по пищеводу усугубит ожог. Показано промывание желудка через зонд. Необходима немедленная госпитализация. Химико-токсикологическое исследование на наличие уксусной кислоты производится только при специальных заданиях или при наличии соответствующих указаний в материалах дела. Объектами ХТА на отравление уксусной кислотой являются: легкие, печень; почки, желудок с содержимым. Изолирование уксусной кислоты из биологического материала проводят перегонкой с водяным паром объектов, предварительно подкисленных серной или фосфорной кислотой, собирая их в приемник с раствором гидроксида натрия (для избегания улетучивания уксусной кислоты). Такой способ извлечения подходит для исследования свежего биологического материала. Полученный дистиллят делят на две части: одну часть исследуют качественными реакциями на наличие ацетат-ионов, а в другой, оттитровывая кислотой избыток гидроксида натрия, определяют количество уксусной кислоты. Второй вариант извлечения уксусной кислоты – извлечение спиртом с последующим подщелачиванием полученного спиртового извлечения и выпариванием его на водяной бане. К полученному сухому остатку добавляют серную или фосфорную кислоты и подвергают перегонке с водяным паром. В этом случае уксусная кислота изолируется более чистой, но вместе с нею изолируются также ацетаты, растворимые в спирте. Для проведения качественных реакций на ацетат-ионы часть дистиллята выпаривают на водяной бане досуха. 1. Реакция с хлоридом железа (III). От прибавления железа (III) хлорида к ацетат-ионам появляется красная окраска, обусловленная образованием основного железа ацетата.
2. Реакция образования индиго. При нагревании уксусной кислоты или ацетатов с солями кальция образуется ацетон, способный в присутствии щелочей взаимодействовать с о-нитробензальдегидом. Конечным продуктом реакции является индиго.
Реакция не специфична, ее способны давать вещества, гидролизующиеся с образованием ацетильной группы. Имеет судебно-химическое значение при отрицательном результате. 3. Образование этилацетата. При нагревании ацетатов с этиловым спиртом в присутствии концентрированной cерной кислоты образуется уксусноэтиловый эфир (этилацетат), обнаруживаемый по характерному запаху, усиливающемуся при выливании реакционной смеси в холодную воду:
Реакция характерна для ацетат-ионов, однако ощущение запаха является субъективным. 4. Образование окиси какодила. Ацетат кальция, образующийся при взаимодействии уксусной кислоты с солями кальция, при нагревании с сухим мышьяковистым ангидридом или солью, мышьяковистой кислоты дает окись какодила, имеющую неприятный запах.
Чувствительность реакции 5-10 мг в 1 мл дистиллята.
|

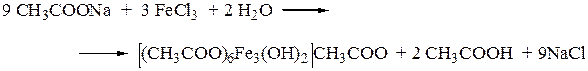 Предел обнаружения составляет 1,25 мг ацетат-ионов в 1 мл дистиллята.
Предел обнаружения составляет 1,25 мг ацетат-ионов в 1 мл дистиллята.