Работа в термодинамике
Ранее, в параграфе 6.1., мы говорили о равновесных состояниях термодинамической системы; в этих состояниях параметры системы одинаковы во всём её объёме. Приступая к рассмотрению работы в термодинамических системах, следует ожидать, что её совершение связано с изменением объёма системы. И тогда возникает вопрос, о каких же процессах идёт речь, если рассмотрению подлежат равновесные состояния? Ответ состоит в следующем: если процесс идёт медленно, то значения параметров состояния во всём объёме можно считать одинаковыми. Понятие «медленно» здесь следует уточнить. Прежде всего, оно связано с понятием «время релаксации» – временем, в течение которого устанавливается равновесие в системе. Нас сейчас интересует время выравнивания давления в системе (время релаксации), когда термодинамической системой совершается работа, связанная с изменением объёма; для однородного газа это время составляет ~ 10–16 с. Очевидно, время релаксации достаточно незначительно по сравнению со временем протекания процессов в реальных термодинамических системах (или по сравнению со временем измерения). Естественно, мы вправе считать, что реальный процесс есть последовательность равновесных состояний и поэтому имеем право, изобразить его линией на графике V, P (рис. 6.1.). Разумеется, по осям координатной системы могут откладываться объём и температура или давление и температура. Поскольку в алгебре, и не только, при построении графиков первой координатной осью читается и записывается х, а затем – у, т. е.«х, у», есть надежда, что читатель, прочитывая «оси координатной системы V, Р», предполагает – по оси х откладывается объём V, а по оси у – давление газа Р. Ознакомимся с видом линий, отображающих графически простейшие процессы в системе координат, по осям которой отложены параметры состояния V, P (возможны иные координатные оси). Выбор координатной системы обусловлен тем, что площадь, ограниченная кривой процесса и двумя крайними координатами для начального и конечного значений объёма, равна работе сжатия или расширения. На рис. 6.2. приведены графики изопроцессов, проведённые из одного и того же начального состояния. Кривая адиабатического процесса (адиабата) идёт круче, чем для изотермического процесса (изотерма). Это обстоятельство можно объяснить на основании уравнения Клапейрона для состояния газов:
Выражая из уравнения состояния Р 1 и Р 2, разность давлений при расширении газа от объёма V 1 до объёма V 2 запишется:

Здесь, как и в уравнении (2), При адиабатическом расширении работа над внешними телами совершается только за счёт внутренней энергии газа, вследствие чего внутренняя энергия, а вместе с ней и температура газа уменьшаются; т. е. в конце адиабатического процесса расширения (см. рис. 6.2.) Т 2 Осознав, что мы имеем дело с равновесными процессами и ознакомившись с их графическим отображением в системе координат (V, P), перейдём к поиску аналитического выражения внешней работы, совершаемой термодинамической системой.
 , то элементарная работа, совершённая системой, запишется , то элементарная работа, совершённая системой, запишется  здесь S – площадь поршня, а здесь S – площадь поршня, а  – изменение объёма системы (рис. 6.3.). При расширении системы внешнее давление не всегда остаётся постоянным, поэтому работа, совершаемая – изменение объёма системы (рис. 6.3.). При расширении системы внешнее давление не всегда остаётся постоянным, поэтому работа, совершаемая  системой при изменении её объёма от V 1 до V 2, должна рассчитываться как сумма элементарных работ, т. е. путём интегрирования: системой при изменении её объёма от V 1 до V 2, должна рассчитываться как сумма элементарных работ, т. е. путём интегрирования:  . Из уравнения работы следует, параметры начального (p 1, V 1) и конечного (p 2, V 2) состояний системы не определяют величину совершаемой внешней работы; необходимо знать ещё и функцию р (V), раскрывающую изменение давления в процессе перехода системы из одного состояния в другое. . Из уравнения работы следует, параметры начального (p 1, V 1) и конечного (p 2, V 2) состояний системы не определяют величину совершаемой внешней работы; необходимо знать ещё и функцию р (V), раскрывающую изменение давления в процессе перехода системы из одного состояния в другое.
В заключение этого параграфа следует заметить, теплообмен между системой и окружающей средой зависит не только от параметров начального и конечного состояний системы, но и от той последовательности промежуточных состояний, через которые проходит система. Это следует из первого закона термодинамики: Q = U 2 – U 1 + A, где U 1 и U 2 определяются только заданием параметров начального и конечного состояний, а внешняя работа A зависит, кроме того, ещё и от самого процесса перехода. Вследствие этого теплота Q, полученная или отданная системой при переходе из одного в другое состояние, не может быть выражена в зависимости только от температуры её начального и конечного состояний. Завершая экскурс в раздел «Термодинамика. Первое начало термодинамики», перечислим его ключевые понятия: термодинамическая система, термодинамические параметры, равновесное состояние, равновесный процесс, обратимый процесс, внутренняя энергия системы, первое начало термодинамики, работа термодинамической системы, адиабатический процесс.
|


 . (2)
. (2) . (3)
. (3) .
. Т 1 (найдите обоснование); при изотермическом же процессе Т 2 = Т 1. Поэтому в формуле (3) разность давлений
Т 1 (найдите обоснование); при изотермическом же процессе Т 2 = Т 1. Поэтому в формуле (3) разность давлений 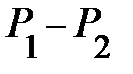 будет больше при адиабатическом расширении, чем при изотермическом расширении (проверьте, проведя преобразования).
будет больше при адиабатическом расширении, чем при изотермическом расширении (проверьте, проведя преобразования).


