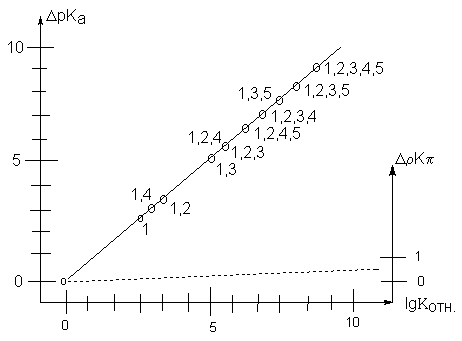Медленной стадией большинства SEAr - реакций является образование  -комплекса (аренониевого иона), поэтому кинетический изотопный эффект водорода в большинстве случаев не проявляется. В этой главе мы рассмотрим общий механизм реакций этого типа, а в следующей главе механизм реакций с изотопным эффектом.
-комплекса (аренониевого иона), поэтому кинетический изотопный эффект водорода в большинстве случаев не проявляется. В этой главе мы рассмотрим общий механизм реакций этого типа, а в следующей главе механизм реакций с изотопным эффектом.
Поскольку и  - комплексы, и
- комплексы, и  - комплексы реально существуют, можно полагать, что оба комплекса образуются в качестве неустойчивых интермедиатов во всех реакциях электрофильного ароматического замещения.
- комплексы реально существуют, можно полагать, что оба комплекса образуются в качестве неустойчивых интермедиатов во всех реакциях электрофильного ароматического замещения.
На рис. 1 приведена идеализированная энергетическая диаграмма для реакции

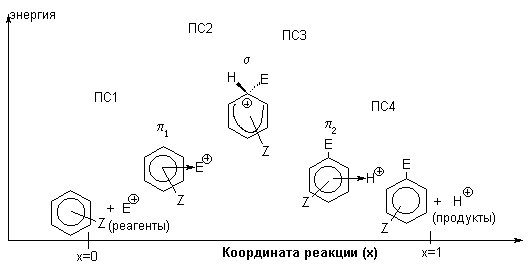
Рис.1 Идеализированная энергетическая диаграмма для реакций электрофильного ароматического замещения. ПС - переходное состояние
На диаграмме изображены два  -комплекса - первый
-комплекса - первый  1 на координате реакции находится до
1 на координате реакции находится до  -комплекса, а второй
-комплекса, а второй  2-после
2-после  -комплекса. Комплекс
-комплекса. Комплекс  1 образуется между исходным ареном и реагентом Е+, а комплекс
1 образуется между исходным ареном и реагентом Е+, а комплекс  2 - между продуктом замещения (ArE) и протоном. Самый высокий энергетический барьер связан с образованием
2 - между продуктом замещения (ArE) и протоном. Самый высокий энергетический барьер связан с образованием  -комплекса.
-комплекса.
 -Комплексы можно рассматривать как "комплексы с переносом заряда". Считается, что связь в них возникает как следствие частичного переноса электрона от арена к электрофилу.
-Комплексы можно рассматривать как "комплексы с переносом заряда". Считается, что связь в них возникает как следствие частичного переноса электрона от арена к электрофилу.
Чтобы выяснить, какая стадия электрофильного замещения - образование  -комплекса или образование
-комплекса или образование  -комплекса - определяет наблюдаемую скорость процесса, обычно изучают влияние заместителей в бензольном кольце на скорость исследуемой реакции и сравнивают его с влиянием этих же заместителей на рКа аренов (табл.1) и на константы устойчивости
-комплекса - определяет наблюдаемую скорость процесса, обычно изучают влияние заместителей в бензольном кольце на скорость исследуемой реакции и сравнивают его с влиянием этих же заместителей на рКа аренов (табл.1) и на константы устойчивости  -комплексов. Если лимитирующей стадией является образование
-комплексов. Если лимитирующей стадией является образование  -комплекса, то переходное состояние "похоже" на
-комплекса, то переходное состояние "похоже" на  -комплекс, скорость электрофильного замещения будет линейно коррелировать с рКа аренов. Если лимитирующей стадией является образование
-комплекс, скорость электрофильного замещения будет линейно коррелировать с рКа аренов. Если лимитирующей стадией является образование  -комплекса, то переходное состояние "похоже" на
-комплекса, то переходное состояние "похоже" на  -комплекс, и скорость замещения будет коррелировать с устойчивостью
-комплекс, и скорость замещения будет коррелировать с устойчивостью  -комплексов.
-комплексов.
В табл. 2 приведены относительные значения основности аренов, констант устойчивости  -комплексов и констант скоростей бромирования и хлорирования метилзамещенных бензолов в 85% уксусной кислоте.
-комплексов и констант скоростей бромирования и хлорирования метилзамещенных бензолов в 85% уксусной кислоте.
Таблица 2
Сравнение основности полиметилбензолов (по данным табл.1) и устойчивости  -комплексов с относительными скоростями их бромирования (Br2 в 85% уксусной кислоте) и хлорирования (Cl2 в уксусной кислоте) при 25оС. В качестве стандартного соединения взят бензол.
-комплексов с относительными скоростями их бромирования (Br2 в 85% уксусной кислоте) и хлорирования (Cl2 в уксусной кислоте) при 25оС. В качестве стандартного соединения взят бензол.
|
|
|
| lg(Карен/Кбензол)
|
| Заместители в бензольном кольце
| Относительная устойчивость  -комплексов с HCl ( -комплексов с HCl (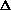 pK pK  ) )
| Относительная основность аренов 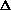 pKа
(табл. 1) pKа
(табл. 1)
| для реакции с бромом
| для реакции с хлором
|
| нет
|
|
|
|
|
| CH3
| 0.18
| 2.9
| 2.78
| -
|
| 1,2-(CH3)2
| 0.26
| 3.9
| 3.72
| 3.62
|
| 1,3-(CH3)2
| 0.31
| 6.0
| 5.71
| 5.6
|
| 1,4-(CH3)2
| 0.22
| 3.5
| 3.4
| 3.3
|
| 1,2,3-(CH3)3
| 0.38
| 6.4
| 6.22
| 5.9
|
| 1,2,4-(CH3)3
| 0.35
| 6.3
| 6.18
| 5.84
|
| 1,3,5-(CH3)3
| 0.42
| 8.8
| 8.28
| -
|
| 1,2,3,4-(CH3)4
| 0.43
| 7.3
| 7.04
| -
|
| 1,2,3,5-(CH3)4
| -
| 9.3
| 8.62
| 8.68
|
| 1,2,4,5-(CH3)4
| -
| 7.0
| 6.45
| -
|
| (CH3)5
| 0.44
| 9.6
| 8.91
| 8.86
|
Данные табл.2 показывают, что скорости реакций бромирования и хлорирования при введении метильных групп увеличиваются почти в той же степени, в которой происходит возрастание основности арена (рис.2). Это означает, что  -комплекс является хорошей моделью переходного состояния для рассматриваемых реакций.
-комплекс является хорошей моделью переходного состояния для рассматриваемых реакций.
В то же время, устойчивость  -комплексов аренов с HCl очень мало зависит от числа метильных заместителей, тогда как скорость хлорирования и бромирования увеличивается в 108раз. Следовательно,
-комплексов аренов с HCl очень мало зависит от числа метильных заместителей, тогда как скорость хлорирования и бромирования увеличивается в 108раз. Следовательно,  -комплекс не может служить моделью переходного состояния в этих реакциях.
-комплекс не может служить моделью переходного состояния в этих реакциях.
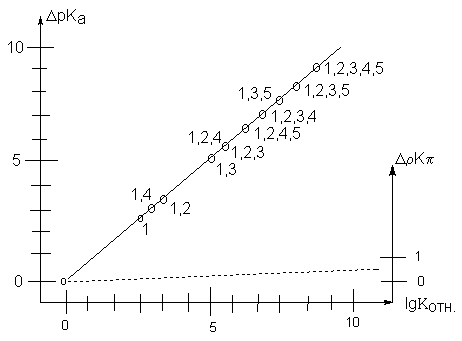
Рис.2 Скорость бромирования толуола, бензола и полиметилбензолов в сравнении с устойчивостью  -комплексов (сплошная линия) и
-комплексов (сплошная линия) и  -комплексов с галогенами (пунктир). Цифры указывают число и положение метильных групп в кольце.
-комплексов с галогенами (пунктир). Цифры указывают число и положение метильных групп в кольце.
Значительное увеличение скорости с введением в бензольное кольцо алкильных групп свойственно, хотя и в несколько меньшей степени, чем при галогенировании, и многим другим реакциям электрофильного замещения. В таких реакциях скорость определяется образованием  -комплекса в качестве интермедиата, и переходное состояние по структуре подобно
-комплекса в качестве интермедиата, и переходное состояние по структуре подобно  -комплексу. Образование
-комплексу. Образование  -комплекса представляет собой быструю обратимую стадию, не оказывающую существенного влияния на скорость реакции в целом. Можно совершенно адекватно описать реакцию, если из кривой потенциальной энергии (рис.1) исключить
-комплекса представляет собой быструю обратимую стадию, не оказывающую существенного влияния на скорость реакции в целом. Можно совершенно адекватно описать реакцию, если из кривой потенциальной энергии (рис.1) исключить  -комплексы и рассматривать лишь положение
-комплексы и рассматривать лишь положение  -комплекса на координате реакции.
-комплекса на координате реакции.

 -комплекса (аренониевого иона), поэтому кинетический изотопный эффект водорода в большинстве случаев не проявляется. В этой главе мы рассмотрим общий механизм реакций этого типа, а в следующей главе механизм реакций с изотопным эффектом.
-комплекса (аренониевого иона), поэтому кинетический изотопный эффект водорода в большинстве случаев не проявляется. В этой главе мы рассмотрим общий механизм реакций этого типа, а в следующей главе механизм реакций с изотопным эффектом. - комплексы, и
- комплексы, и 

 pK
pK