Классификация заместителей
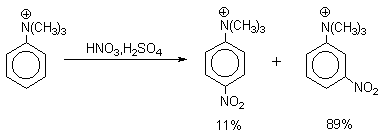
Монозамещенные бензолы С6Н5Х могут быть более или менее реакционноспособны, чем сам бензол. Если в реакцию ввести эквивалентную смесь С6Н5Х и С6Н6, то замещение будет происходить селективно: в первом случае в реакцию будет вступать преимущественно С6Н5Х, а во втором случае - преимущественно бензол. В настоящее время заместители делят на три группы с учетом их активирующего или дезактивирующего влияния, а также ориентации замещения в бензольном кольце.
Эти две группы (1 и 2) заместителей называют ориентантами I-го рода.
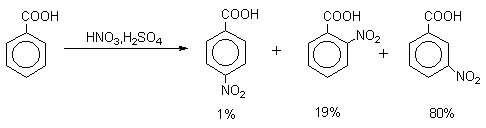
Естественно, что существуют и группировки атомов промежуточного характера, обусловливающие смешанную ориентацию. К ним, например, относятся: CH2NO, CH2COCH3, CH2F, CHCl2, CH2NO2, CH2CH2NO2, CH2CH2NR3+, CH2PR3+, CH2SR2+ и др. Приведем некоторые типичные примеры влияния ориентантов I и II-го рода:
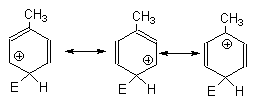
2.6.3. Ориентация как отражение свойств Наиболее часто ориентацию электрофильного замещения в бензольном кольце объясняют с точки зрения стабильности образующегося в качестве промежуточной частицы аренониевого иона. При этом предполагают, что переходное состояние медленной стадии по структуре близко или идентично аренониевому иону ( В качестве первого примера рассмотрим влияние сильных активирующих заместителей для орто- и мета- или пара-замещения в анизоле. Для орто-замещения в анизоле две граничные формулы аренониевого иона представляют собой вторичный карбокатион, а третья - третичный, где положительный заряд дополнительно стабилизирован за счет участия неподеленной пары 2р-электронов атома кислорода СН3О-группы с образованием оксониевой структуры:
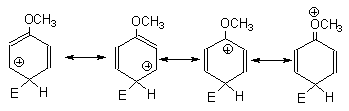
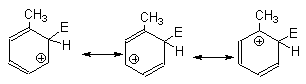
Для пара-замещения в анизоле две граничные формулы также являются вторичными карбокатионами, а третья - третичным, стабилизированным соседней метоксильной группой:
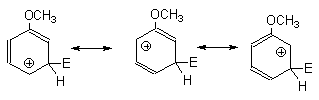
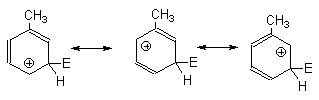
Стабилизация циклогексадиенильного катиона за счет СН3О-группы облегчает замещение в орто- и пара-положениях анизола по сравнению с бензолом и ориентирует входящую группу Е именно в эти два положения кольца. Для мета-замещения в анизоле подобная стабилизация невозможна, так как ни в одной из граничных формул положительный заряд не находится у атома углерода, несущего метоксигруппу.
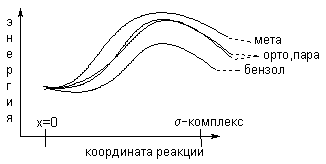
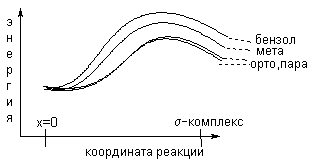
Более того, для анизола мета-аренониевый ион дестабилизирован по сравнению с циклогексадиенильным катионом за счет (-I)-эффекта СН3О-группы. Соответствующие энергетические кривые для орто-, пара- и мета-замещения в анизоле, а также кривая для бензола приведены на рис.3.
Рис.3 Селективность электрофильного замещения в анизоле Аналогичная картина наблюдается и для замещения в феноле, анилине, моно- и диалкиланилинах и других аренах, содержащих (+М)-заместители. Теперь рассмотрим реакции замещения в толуоле и других алкилбензолах. Для орто- и пара-замещения две граничные формулы аренониевого иона соответствуют вторичному карбокатиону, а третья - третичному, стабилизированному за счет гиперконьюгации с метильной группой. Поэтому переходное состояние для орто- и пара-замещения в толуоле обладает меньшей энергией по сравнению с переходным состоянием для мета-замещения в бензоле, где все три граничные структуры отвечают вторичным карбокатионам.
Каждая из этих граничных структур стабилизирована с помощью (+I)-эффекта СН3-группы, но эта стабилизация невелика. Поэтому мета-положение в толуоле более активно в реакциях замещения по сравнению с бензолом, но менее активно, чем его орто- и пара-положения. Соответствующие энергетические кривые для реакций замещения в орто- и мета-положения толуола по сравнению с бензолом приведены на рис.4.
Рис.4 Селективность электрофильного замещения в толуоле Для замещения в галогенбензолах положение энергетических кривых отличается от аналогичных кривых для замещения в анизоле, тогда как граничные формулы для аренониевых ионов галогенбензолов и анизола аналогичны. При замещении в мета-положении карбокатионы, соответствующие двум последним граничным формулам, сильно дестабилизированы за счет электростатического взаимодействия карбокатионного центра с положительным концом диполя связи углерод-галоген.
Поэтому мета-замещение в галогенбензолах сильно дезактивировано по сравнению с бензолом. Граничные структуры для замещения в орто- и пара-положения также дестабилизированы по сравнению с бензолом электростатическим взаимодействием диполя углерод-галоген с карбокатионным центром. Однако в одной из граничных структур для замещения в орто- и пара-положениях реализуется структура
Галогенониевые ионы менее стабильны, чем оксониевые или иминиевые ионы и вклад этой структуры не компенсирует дестабилизирующий эффект электростатического отталкивания диполя С
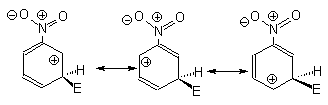
Рис.5 Селективность электрофильного замещения в хлорбензоле Влияние мета-ориентирующих заместителей проиллюстрируем на примере нитробензола. Ниже приведены граничные формулы аренониевого иона для орто-, пара- и мета-замещения в нитробензоле.
Во всех граничных формулах происходит сильное электростатическое отталкивание между карбокатионным центром и положительным концом диполя связи С
Рис.6 Селективность электрофильного замещения в нитробензоле
|


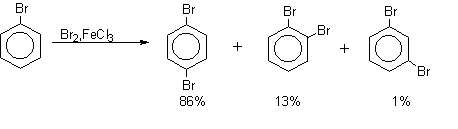


 -комплекса
-комплекса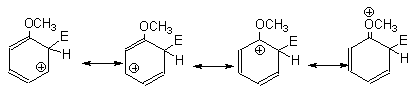

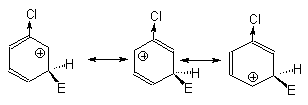
 -галогензамещенного карбокатиона, для которого возможна стабилизация с положительным зарядом на атоме галогена.
-галогензамещенного карбокатиона, для которого возможна стабилизация с положительным зарядом на атоме галогена.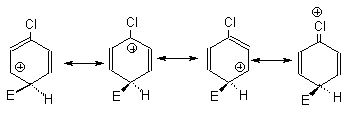
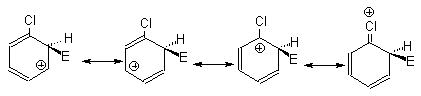
 + -Х
+ -Х