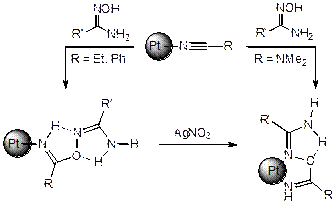СИНТЕЗ АНАЛОГОВ СТЕРОИДНЫХ ЭСТРОГЕНОВ, СОДЕРЖАЩИХ МЕТИЛЬНЫЕ ГРУППЫ В КОЛЬЦЕ D
Богаутдинов Р.П. Санкт-Петербургский государственный университет, Санкт-Петербург, Россия. Студент V курса. r.bogautdinov@gmail.com Научный руководитель: Морозкина С.Н.
Литература: [1] Берштейн, Л. М., Гормональный канцерогенез.– СПб: Наука, 2000, 199 с. [2] McDougal A., Gupta M.S. et al. Cancer Lett. 151, 169 (2000 ). [3] Römer W., Oettel M. et al Steroids 62, 304-310 (1997). НУКЛЕОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ АМИДОКСИМОВ К НИТРИЛАМ, АКТИВИРОВАННЫМ ПЛАТИНОЙ(II)
Болотин Д.С. Санкт-Петербургский государственный университет, Санкт-Петербург, Россия. Студент V курса. dmitriy.s.bolotin@gmail.com Научный руководитель: Бокач Н.А.
Реакции нуклеофильного присоединения оксимной группы к нитрильным лигандам известны как для комплексов металлов в высших (ReIV, RhIII, and PtIV), так и в промежуточных (PtII, PdII, NiII) степенях окисления. Вследствие существенно меньшей активации нитрильных субстратов, реакции с участием металлоцентров в промежуточных степенях окисления требуют более жестких условий и протекают с меньшими выходами. Данные реакции могут промотироваться наличием электроноакцепторной группы в нитриле или донорных групп в оксиме. Всего три работы [1, 2, 3] посвящены изучению реакций нуклеофильного присоединения оксимов к диалкилцианамидам и нитрилам, координированным к платине(II). В случае диалкилцианамидов присоединение диалкилкетоксимов происходит только при дополнительной активации кислотами Льюиса [1], тогда как присоединение к нитрилам происходит только при наличии акцепторных групп в координированном субстрате и в более жестких условиях (50 ºC или микроволновое излучение) [2, 3]. Ранее [4] нами было установлено, что амидоксимы R’C(=NOH)NH2 являются более реакционоспособными по отношению к нуклеофильному присоединению к нитрилам, координированным к платине(IV), чем диалкилкетоксимы. Мы распространили рассматриваемую реакцию на менее активные субстраты – комплексы платины(II).
Комплексы цис - и транс -[PtCl2(RCN)2] (R=Et, Ph, NMe2) реагируют с одним и двумя эквивалентами амидоксимов R’C(=NOH)NH2 (R’=Me, Ph) во всех возможных соотношениях, образуя продукты присоединения. Было обнаружено, что из диметилцианамидных производных формируются хелатные продукты [PtCl(NCNMe2)(H N =C(NMe2)O N =C(R')NH2)]Cl и [Pt(H N =C(NMe2)O N =C(R')NH2)2]Cl2, в то время, как из нитрильных – не хелатные [PtCl2(RCN)(H N =C(R)ON=C(R')NH2)] и [PtCl2(H N =C(R)ON=C(R')NH2)2]. В рамках данной работы обсуждается относительная реакционная способность координированных нитрильных субстратов, а также сравнивается реакционная способность амидоксимов с кетоксимами R2CNOH и альдоксимами RC(NOH)H. Было обнаружено, что вследствие + М эффекта NH2 группы амидоксимы являются более сильными HO-нуклеофилами, чем кетоксимы и альдоксимы.
Литература: [1] C. M. P. Ferreira, M. F. C. Guedes da Silva, J. J. R. Frausto da Silva, A. J. L. Pombeiro, V. Y. Kukushkin and R. A. Michelin, Inorg. Chem. 40, 1134-1142 (2001) [2] J. Lasri, M. A. l. J. r. Charmier, M. F. t. C. Guedes da Silva and A. J. L. Pombeiro, Dalton Transactions, 5062 (2006) [3] J. Lasri, M. F. C. Guedes da Silva, M. A. J. Charmier and A. J. L. Pombeiro, Eur. J. Inorg. Chem., 3668-3677 (2008) [4] D. S. Bolotin, N. A. Bokach, M. Haukka and V. Y. Kukushkin, ChemPlusChem 77, 31-40 (2012)
|

 Половые гормоны являются одними из важнейших низкомолекулярных регуляторов в человеческом организме. На основе аналогов женских половых гормонов (эстрогенов) на данный момент создан ряд лекарственных препаратов, обладающих весьма широким спектром положительных воздействий (антиоксидантное, остео-, кардио-, нейропротекторное и другие). Однако есть и обратная сторона медали – гормональная (утеротропная) активность данных препаратов, которая может способствовать развитию гормон-зависимых раковых опухолей (главным образом, рака молочной железы у женщин) [1]. Целями данной работы являлись усовершенствование методов синтеза определенной группы аналогов – модифицированных эстрогенов, содержащих метильные группы в кольце D стероидного скелета.
Половые гормоны являются одними из важнейших низкомолекулярных регуляторов в человеческом организме. На основе аналогов женских половых гормонов (эстрогенов) на данный момент создан ряд лекарственных препаратов, обладающих весьма широким спектром положительных воздействий (антиоксидантное, остео-, кардио-, нейропротекторное и другие). Однако есть и обратная сторона медали – гормональная (утеротропная) активность данных препаратов, которая может способствовать развитию гормон-зависимых раковых опухолей (главным образом, рака молочной железы у женщин) [1]. Целями данной работы являлись усовершенствование методов синтеза определенной группы аналогов – модифицированных эстрогенов, содержащих метильные группы в кольце D стероидного скелета. Подобные соединения, как ожидается, будут обладать целым рядом интересных свойств. Метильные группы в кольце D снижают риск образования канцерогенных метаболитов из данных препаратов [2], а метильная группа в положении 1 предотвращает повреждение метаболитами ДНК и последующую индукцию раковых заболеваний. Двойная связь, введенная в положение 8(9), придает аналогам сильное антиоксидантное [3] и остеопротекторное свойства, в то время как неприродное (8α) цис-сочленение колец B и C понижает гормональную активность препаратов. На данный момент по схеме Торгова-Ананченко нами получено несколько искомых аналогов (Рис. 1). Синтезированы модифицированные стероидные эстрогены с различными сочленениями колец (как природным, так и неприродным), а также частично прогидрированные аналоги.
Подобные соединения, как ожидается, будут обладать целым рядом интересных свойств. Метильные группы в кольце D снижают риск образования канцерогенных метаболитов из данных препаратов [2], а метильная группа в положении 1 предотвращает повреждение метаболитами ДНК и последующую индукцию раковых заболеваний. Двойная связь, введенная в положение 8(9), придает аналогам сильное антиоксидантное [3] и остеопротекторное свойства, в то время как неприродное (8α) цис-сочленение колец B и C понижает гормональную активность препаратов. На данный момент по схеме Торгова-Ананченко нами получено несколько искомых аналогов (Рис. 1). Синтезированы модифицированные стероидные эстрогены с различными сочленениями колец (как природным, так и неприродным), а также частично прогидрированные аналоги.