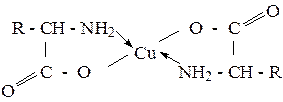Аминокислоты, белки
Аминокислотами называются соединения, в молекуле которых содержатся одновременно аминные и карбоксильные группы. Аминокислоты проявляют свойства, характерные как для кислот, так и для аминов. Кроме того, аминокислоты обладают специфическими свойствами, характерными для соединений содержащих две различные по своей природе функциональные группы. В связи с наличием аминогрупп аминокислоты дают соли с кислотами, например:
При действии азотистой кислоты на аминокислоты реакция протекает так же, как и в случае аминов. Из первичных аминов образуются спирты, из аминокислот - оксикислоты. В качестве ацилирующих агентов применяют галогенангидриды и ангидриды кислот. При алкилировании галогеналкилами образуются моно-, ди-, триалкилпроизводные. Аминокислоты, как и алифатические кислоты, образуют соли, сложные эфиры, галогенангидриды и другие производные. Особую группу составляют реакции, связанные с наличием и взаимными влиянием амино- и карбоксильных групп. Это отношение аминокислот к нагреванию. a-Аминокислоты при нагревании, отщепляя воду, образуют циклические соединения – дикетопиперазины. b-Аминокислоты при нагревании выделяют аммиак и превращаются в непредельные кислоты. g- и d-Аминокислоты легко отщепляют воду и циклизуются, образуя циклические амиды – лактамы. a-Аминокислоты при взаимодействии с гидроксидом меди (II) образуют комплексные соли:
Аминокислоты могут вступать в реакции поликонденсации с образованием пептидов и полипептидов. Повторяющаяся в полипептидной цепи группа атомов
называется пептидной, а связь C – N – пептидной связью. Согласно общепринятой теории молекула белка состоит из остатков a-аминокислот, связанных между собой пептидными связями:
Качественными реакциями на белки являются: а) биуретовая реакция; б) ксантопротеиновая реакция; в) реакция Миллона; г) нингидринная реакция.
|