Характеристики процесса возбуждения на клеточном уровне
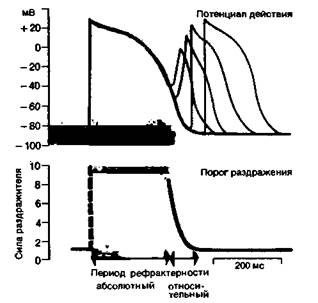
Как в нервных клетках и в волокнах скелетных мышщ, потенциал действия (ПД) в кардиомиоцитах начинается с быстрой реверсии мембранного потенциала от уровня покоя (примерно —90 мВ) до пика ПД (примерно +30 мВ) (рис. 19.4). За этой фазой быстрой деполяризации, продолжительность которой составляет лишь 1-2 мс, следует более длительная фаза плато - специфическая особенность клеток миокарда. Затем наступает фаза реполяризации, по окончании которой восстанавливается потенциал покоя. Длительность потенциала действия кардиомиоцитов составляет 200-400 мс, т. е. более чем в 100 раз превышает соответствующую величину для скелетных мышц и нервных волокон. Как будет показано ниже, это имеет большое функциональное значение. Ионные механизмы возбуждения. Потенциал действия возникает в результате изменений мембранного потенциала, проницаемости для различных ионов и ионных потоков. Основы ионной теории возбуждения подробно рассмотрены в гл. 1; здесь же мы кратко остановимся на некоторых положениях этой теории применительно к особенностям клеток миокарда [2, 9, 20, 23]. Потенциал покоя этих клеток создается преимущественно за счет К+ -потенциала, поддерживаемого благодаря работе электрогенного натриевого насоса. Как и в нервных клетках, быстрая восходящая фаза ПД кардиомиоцитов обусловлена коротким, но значительным повышением проводимости для натрия (gNa), что приводит к лавинообразному входу Na+ (рис. 19.4). Однако этот начальный входящий ток Na+ быстро инактивируется (в этом кардиомиоциты также сходны с нервными клетками), поэтому значительное замедление реполяризации в клетках миокарда обусловлено иными механизмами. К ним относятся Π медленно развивающееся увеличение проводимости для Ca2 + (gCa), в результате которого возникает деполяризующий входящий ток кальция (медленный входящий ток) [21]; 2) снижение проводимости для К+ (gK), возникающее при деполяризации и уменьшающее реполя- 458 ЧАСТЬ V. КРОВЬ И СИСТЕМА КРОВООБРАЩЕНИЯ ризуюший выходящий ток К+ [2, 23]. Реполяризация в клетках миокарда обусловлена постепенным уменьшением gCa, а также тем, что при увеличении отрицательного мембранного потенциала повышается gK. Уменьшение gCa приводит к снижению медленного входящего тока, а повышение gK - к увеличению выходящего тока К+. В состоянии покоя деполяризующие и реполяризующие токи находятся в равновесии. Механизмы, лежащие в основе этого медленного входящего тока Са2+ и быстрого входящего тока Na+, различаются по многим параметрам, в том числе по временному ходу, зависимости от потенциала и чувствительности к блокирующим агентам. Так называемый быстрый натриевый канал блокируется тетродотоксином, а медленный кальциевый ионами Cd2+ и органическими антагонистами Са2+ (например, верапамилом, нифедипином, дилтиаземом) [5]. Порог активации натриевого канала равен примерно —60 мВ, а кальциевого - около —30 мВ. При деполяризации мембраны до —40 мВ быстрый натриевый канал инактивируется. При этом под действием сверхпороговых раздражителей могут возникать так называемые кальциевые потенциалы действия, имеющие более пологий передний фронт (так как медленный входящий ток в этом случае обусловливает не только плато, но и передний фронт ПД) и меньшую скорость распространения («медленный ответ» [3]). Период рефрактерности. Определенным фазам цикла возбуждения в сердце, как и в других возбудимых тканях, соответствуют периоды невозбудимо-
сти (абсолютной рефрактерности) и сниженной возбудимости (относительной рефрактерности). На рис. 19.5 показаны эти периоды и их связь с различными фазами ПД. Во время периода абсолютной рефрактерности клетка невозбудима; затем следует период относительной рефрактерности, в течение которого возбудимость постепенно восстанавливается. Таким образом, чем больше сила повторного стимула, тем раньше можно вызвать очередной потенциал действия. ПД, возникающие в начальной стадии периода относительной рефрактерности, нарастают более полого, имеют меньшую амплитуду и длительность (рис. 19.5). Рефрактерность связана главным образом с инактивацией быстрых натриевых каналов, наступающей при длительной деполяризации (с. 33). Эти каналы начинают восстанавливаться лишь после того, как мембрана реполяризуется примерно до уровня —40 мВ. Таким образом, продолжительность рефрактерного периода, как правило, тесно связана с длительностью потенциала действия. Если ПД укорачивается или удлиняется, этому соответствуют такие же изменения периода рефрактерности. Однако препараты, обладающие местным анестезирующим действием, могут подавлять быстрые натриевые каналы и замедлять восстановление проницаемости после инактивации, вызывая тем самым удлинение рефрактерного периода, но не влияя на продолжительность потенциала действия. Функциональное значение периода рефрактерности. Длительный рефрактерный период предохраняет миокард от слишком быстрого повторного возбуждения. Такое возбуждение могло бы нарушить нагнетательную функцию сердца. Вместе с тем фаза рефрактерности препятствует круговому движению возбуждения по миокарду, которое привело бы к нарушению ритмичного чередования сокращения и расслабления. В норме рефрактерный период клеток миокарда больше, чем время распространения возбуждения по предсердиям или желудочкам. Поэтому после того, как волна возбуждения из САузла или гетеротопного очага охватит полностью весь миокард, она угасает; обратный вход этой волны невозможен, так как все сердце находится в состоянии рефрактерности. Зависимость длительности потенциала действия от частоты. Как показано на рис. 19.5, потенциал действия, возникающий сразу после окончания периода относительной рефрактерности предыдущего цикла возбуждения, характеризуется обычной крутизной переднего фронта и амплитудой. Однако длительность ПД значительно уменьшена. Таким образом, существует тесная связь между продолжительностью потенциала действия и длительностью интервала между началом этого ПД и концом предыдущего, т. е. между длительностью и частотой ПД. На рис. 19.6 приведена оригинальная запись для поло- ГЛАВА 19. ФУНКЦИЯ СЕРДЦА 459
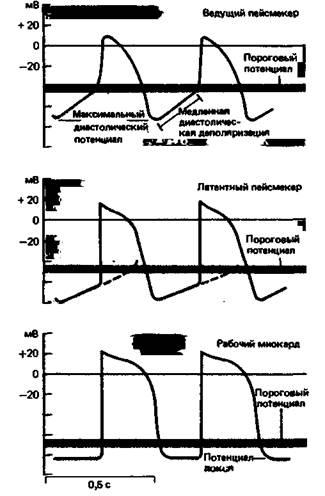
ски желудочка человека, иллюстрирующая эту зависимость. Описанный эффект обусловлен главным образом тем, что gK после окончания реполяризации еще повышена и лишь через некоторое время постепенно возвращается к исходному уровню (рис. 19.4). В том случае, если интервал между ПД мал. это повышение проницаемости для К+ приводит к ускорению реполяризации в очередных циклах возбуждения. Клеточные механизмы возникновения возбуждения в сердце. Клетки рабочего миокарда предсердий и желудочков не обладают автоматизмом. Потенциалы действия в них возникают лишь под влиянием распространяющегося возбуждения: от возбужденных участков к невозбужденным течет ток, вызывающий деполяризацию последних. Когда в результате этой деполяризации мембранный потенциал достигает критического (порогового) значения, возникает потенциал действия (с. 30). Что же касается клеток сердца, обладающих автоматизмом, то они спонтанно деполяризуются до критического уровня. Это явление можно наблюдать при прямой внутриклеточной регистрации мембранных потенциалов клеток пейсмекера. Как видно из рис. 19.7, в таких клетках за фазой реполяризации следует фаза медленной диастолической деполяризации, начинающаяся сразу по достижении максимального диастолического потенциала и приводящая к снижению мембранного потенциала до порогового уровня и возникновению ПД. В отличие от потенциала действия медленная диастолическая деполяризация (пейсмекерный потенциал. препотенциал) - это местное, нераспространяющееся возбуждение. Истинные и латентные водители ритма. В норме ритм сердечных сокращений задают лишь несколько клеток синоатриального узла - так называемые истинные водители ритма. Все остальные клетки проводящей системы разряжаются, как и рабочий миокард, под действием распространяющегося возбуждения. Эти клетки называют латентными (скрытыми, потенциальными) водителями ритма. Потенциал действия в них возникает под влиянием токов от возбужденных участков до того, как в результате их собственной медленной диастолической деполяризации их мембранный потенциал достигнет порогового уровня. На рис. 19.7, где приведены потенциалы действия истинного и латентного пейсмекеров, показано, каким образом латентный водитель ритма может взять на себя ведущую функцию при выключении истинного водителя ритма. В связи с тем что в латентных водителях ритма медленная диастолическая деполяризация позже достигает порогового уровня, частота их разрядов ниже. Клетки же рабочего миокарда не обладают спонтанной деполяризацией, и их потенциалы действия, возникающие под влиянием внешних токов, характеризуются крутым передним фронтом на фоне постоянного потенциала покоя (рис. 19.7, нижняя кривая). Ионные механизмы пейсмекерного потенциала. В соответствии с современными представлениями медленная диастолическая деполяризация в синоатриальиом узле обусловлена иными механизмами, нежели в желудочковой проводящей системе [17]. Во-первых, для клеток СА-узла характерен более высокий постоянный фоновый натриевый ток, препятствующий достижению равновесного калиевого потенциала Ек. В связи с этим мембранный потенциал этих клеток постоянно низок, и быстрые натриевые каналы (даже если они в этих клетках имеются) инактивированы. Во время фазы реполяризации потенциала действия проницаемость мембраны для калия увеличивается, становясь выше уровня покоя. В результате мембранный потенциал приближается к равновесному калиевому потенциалу ЕK и достигает максимального диастолического значения (рис. 19.7). Затем gK постепенно снижается до уровня покоя и мембранный потенциал все более отличается от ЕK, достигая в конечном счете уровня, при котором активируется медленный входящий ток. отвечающий за передний фронт ПД в данных клетках (таким образом, их потенциалы действия сходны с ПД деполяризованных клеток желудочков", см. выше). Сходные механизмы действуют и в АВ-узле. Что же касается клеток желудочковой проводящей системы, то у них фоновая натриевая проницаемость в норме мала. В связи с этим мембранный потенциал сразу после окончания ПД достигает довольно высокого уровня, что обусловливает значительное восстановление быстрого натриевого тока. Далее начинается диастолическая деполяризация, которая в этих клетках обусловлена особым ионным каналом, не действующим в клетках СА-узла; этот канал активируется лишь при существенной поляризации и пропускает как Na+, так и К+ [16]. Передний фронт ПД в этих клетках крутой, так как создается быстрым входящим натриевым током. 460 ЧАСТЬ V. КРОВЬ И СИСТЕМА КРОВООБРАЩЕНИЯ
Эктопические водители ритма. Способностью к спонтанному возбуждению обладают более примитивные клетки, а не высокоспециализированные рабочие кардиомиоциты. На ранних стадиях эмбрионального развития этой способностью обладают все клетки закладки сердца. По мере дифференцировки клеток предсердий и желудочков автоматизм у них исчезает и появляется устойчивый высокий потенциал покоа. Однако при некоторых патологических состояниях, связанных с частичной деполяризацией мембран (катэлектротон, растяжение, гипокалиемия, действие ионов Ва2+), стабильность потенциала покоя у этих клеток утрачивается, и в результате в них может появляться диастолическая деполяризация, характерная для водителей ритма. При определенных условиях их разряды могут влиять на ритм сердца. Вместе с тем деполяризация, вызванная повышением уровня К+, не приводит к повышению автоматизма, так как одновременно увеличивается проводимость для К+, что подавляет спонтанную активность. Центр автоматизма, не относящийся к проводящей системе, называется эктопическим очагом (или фокусом). Разновидности ПД в клетках сердца. В различных участках сердца потенциалы действия характеризуются определенными особенностями. ПД для некоторых отделов сердца приведены на рис. 19.8, причем потенциалы верхних отделов изображены в верхней части рисунка, а нижних-в нижней. Интервал от нулевой вертикальной линии до переднего фронта ПД соответствует времени задержки возбуждения того или иного отдела по отношению к синусному узлу. По мере удаления от синусного узла того или иного отдела проводящей системы наклон кривой медленной диастолической деполяризации клеток становится все менее крутым. Крутизна переднего фронта и амплитуда потенциала действия в клетках CA- и АВ-узлов существенно ниже, чем в остальных отделах проводящей системы. Длительность плато и соответственно рефрактерного периода в рабочих клетках предсердий меньше, чем в миокарде желудочков. Окончания волокон Пуркинье обладают весьма длительными потенциалами действия и поэтому играют роль «частотного фильтра», препятствующего слишком
ГЛАВА 19. ФУНКЦИЯ СЕРДЦА 461 частым сокращениям желудочков при чрезмерно высокой частоте возбуждения предсердий. Связь между возбуждением и сокращением (электромеханическое сопряжение)
|