Физико-химия растворов полимеров.
Специфика свойств растворов полимеров обусловлена прежде всего большими размерами и гибкостью макромолекул. Рассмотрим некоторые особенности растворов полимеров. 1. Растворы полимеров имеют формальное сходство с коллоидными системами на основе низкомолекулярных веществ. Общим их формальным признаком является наличие в низкомолекулярной жидкости больших по размеру частиц: макромолекул в случае раствора полимера и близких к ним по размерам частиц дисперсионного вещества в случае коллоидных систем на основе низкомолекулярных соединений (эмульсий, суспензий). Несмотря на это формальное сходство, истинные растворы полимеров и коллоидные системы имеют ряд принципиальных различий. К их числу относятся термодинамическая устойчивость растворов полимеров и термодинамическая неустойчивость коллоидных систем; однофазность растворов полимеров и двухфазность коллоидных систем; агрегативная устойчивость растворов полимеров и агрегативная неустойчивость коллоидных систем; обратимость свойств растворов полимеров и необратимость свойств в случае коллоидных систем. Образование полимерами истинных растворов не исключает возможности получения на их основе коллоидных систем. Типичными примерами таких систем являются сок каучуконосных растений (сок гевеи — стабилизированная белковыми соединениями дисперсия натурального каучука в воде, называемая латексом), а также получаемые в промышленности латексы синтетических полимеров (полибутадиеновые каучуки, полистирол, поливинилхлорид и др.). 2.Растворы полимеров имеют высокую вязкость даже при большом разбавлении, например при концентрациях менее 1%. Эта особенность характерна только для полимерных растворов и обусловлена длинноцепочечным строением их макромолекул. Ограниченное набухание - процесс смешения полимера и растворителя, ограниченный только стадией поглощения растворителя полимером: самопроизвольного растворения полимера не происходит, так как цепи не могут быть полностью отделены друг от друга. При ограниченном набухании образуются две сосуществующие фазы: набухший полимер и чистый растворитель (возможно, разбавленный раствор в нем полимера, если последний частично растворим). Эти фазы разделены поверхностью раздела и находятся в равновесии. Ограниченно могут набухать как линейные, так и сетчатые полимеры. Линейные полимеры в определенных условиях могут набухать ограниченно, но при изменении этих условий ограниченное набухание может перейти в неограниченное. При наличии в полимере пространственной сетки химических связей образование истинного раствора без разрушения этих связей невозможно; такие полимеры могут только ограниченно набухать. Способность полимеров к ограниченному набуханию оценивают по степени набухания, которая представляет собой отношение объема поглощенной полимером жидкости (или ее пара) к единице массы или объема полимера:
где m0 и V0 — масса и объем исходного полимера; m и V — масса и объем полимера, набухшего до равновесного состояния. Поскольку растворы полимеров образуются самопроизвольно, их образование, как и всякий самопроизвольный процесс, сопровождается уменьшением энергии Гиббса, т.е. ΔGсм = (Gр-ра – ΣGкомп) < 0 где ΔGсм – изменение энергии Гиббса при растворении; Gр-ра – энергия Гиббса раствора; ΣGкомп – сумма энергий Гиббса компонентов раствора до растворения. Энергия Гиббса связана с изменением энтальпии и энтропии процесса уравнением ΔGсм = ΔНсм - Т ΔSсм где ΔНсм = Нр-ра – ΣНкомп и ΔSсм = Sр-ра – ΣSкомп – изменения соответственно энтальпии и энтропии системы при растворении, т.е. энтальпия и энтропия смешения. Из условия ΔG < 0 следует, что самопроизвольное растворение полимера реализуется в нескольких вариантах. 1. ΔНсм < 0 и ΔSсм > 0. Растворение экзотермическое и сопровождается возрастанием энтропии. При этом энергия взаимодействия между разнородными молекулами больше, чем между однородными (в расчёте на 1 моль растворителя и 1 моль звеньев полимера). 2. ΔНсм < 0 и ΔSсм < 0 при условии |ΔНсм| > |TΔSсм|. Растворение также экзотермическое, но сопровождается уменьшением энтропии. Это может происходить, например, при растворении полярных полимеров в полярных растворителях. 3. ΔНсм > 0 и ΔSсм > 0 при условии |ΔНсм| < |TΔSсм|. Растворение эндотермическое и сопровождается возрастанием энтропии. Это наблюдается в неполярных растворителях. 4. ΔНсм = 0 и ΔSсм > 0. Растворение атермическое и сопровождается возрастанием энтропии. Это наблюдается, например, при растворении полимера в соответствующем ему гидрированном мономере (полиизобутилена в изооктане, поливинилацетата в этилацетате и др.). Осмотическое давление растворов полимеров. Если разделить раствор и растворитель полупроницаемой перегородкой, через которую могут диффундировать только молекулы растворителя, то вследствие неравенства химических потенциалов растворителя по обе стороны перегородки его молекулы начнут перемещаться в раствор, повышая его уровень и гидростатическое давление на перегородку. Следовательно, стремление молекул растворителя к самопроизвольному проникновению в раствор, вызванное неравенством где р и р0 — давление на перегородку со стороны раствора и растворителя соответственно в условиях равновесия.
|

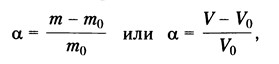
 μ i < 0, можно оценить давлением π, называемым осмотическим:
μ i < 0, можно оценить давлением π, называемым осмотическим: 


