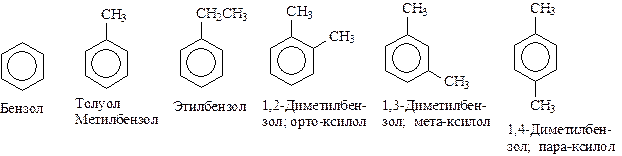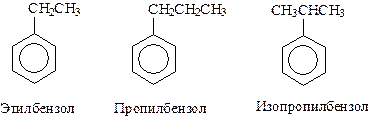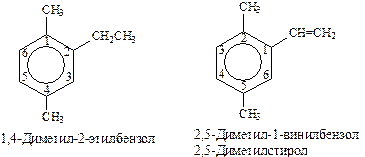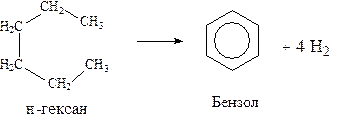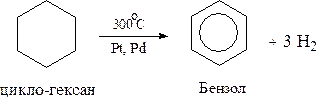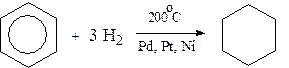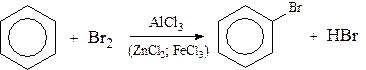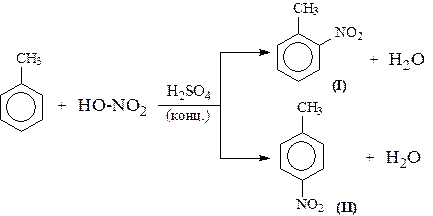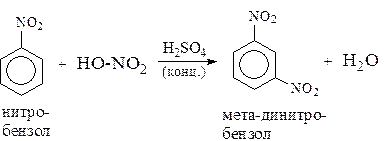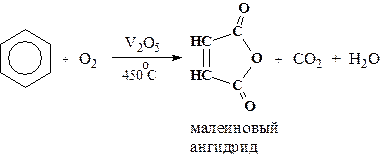Ароматические углеводороды (арены)
Общая формула аренов СnН2n-6. Это углеводороды, в молекулах которых присутствует бензольное кольцо:
Простейшие представители этого класса углеводородов:
Названия гомологов бензола строятся следующим образом: - при наличии одного заместителя в ароматическом кольце называют сначала заместитель, затем добавляют бензол:
- при наличии двух заместителей положение заместителей нумеруется. При этом может быть три варианта взаимного расположения заместителей:
Кроме того, для обозначения положений 1, 2- может применяться приставка орто-, для 1, 3-- приставка мета-, для 1, 4- - приставка пара-; - при наличии трех и более заместителей также нумеруется положение заместителей. Из возможных порядков заместителей выбирается тот, при котором сумма номеров заместителей будет наименьшей. Например:
Природные источники ароматических углеводородов: а) Каменноугольная смола, которая получается при сухой перегонке каменного угля. б) Нефть. Содержание ароматических углеводородов в нефтях составляет от 5 до 35%. Из синтетических методов получения ароматических углеводородов нельзя не отметить следующие: 1. Получение из алканов, имеющих в цепи не менее шести атомов углерода, реакцией дегидроциклизации. Эту реакцию проводят при температуре 450-500°С на окисных катализаторах (Сr2O3 на Аl2О3).
2. При температуре 300°С на катализаторах Pt, Pd или Ni циклогексан дегидрируется до бензола:
Последние две реакции являются основными, за счет которых получаются ароматические углеводороды в промышленном процессе каталитического риформинга (платформинга). 3. При пропускании ацетилена над активированным углем при 600°С получается бензол. 4. Гомологи бензола можно получить алкилированием бензольного кольца по реакции Фриделя- Крафтса:
В бензольном кольце имеется замкнутая система из 6 p-электронов, равномерно распределенных по всей плоскости кольца. Этим объясняются специфические свойства ароматических углеводородов. По строению бензол и его гомологи являются непредельными соединениями. Однако в обычных условиях бензол не присоединяет бром (не обесцвечивает бромную воду), не окисляется перманганатом калия (КМnO4). В отдельных случаях бензол способен к реакциям присоединения, однако они идут в более жестких условиях для бензола, чем для непредельных углеводородов. Так, молекула бензола присоединяет 3 молекулы водорода с образованием циклогексана, однако эта реакция идет при температуре 180-200°С на катализаторах Ni, Pt, Pd.
Но в целом для ароматических углеводородов более характерны реакции замещения. 1. В присутствии катализаторов хлор и бром замещают атомы водорода в молекуле бензола
2. С НСl и НВr бензол не реагирует, а с концентрированной H2SO4 происходит замещение атома водорода на сульфогруппу (-SО3Н) и образуется бензолсульфокислота:
Эта реакция идет при комнатной температуре. 3. При действии на бензол смеси конц. Н2SО4 и конц. НNO3 (нитрующей смеси) происходит замещение в бензоле атома водорода на нитрогруппу -NO2:
Необходимо отметить, что если в бензольном кольце уже есть заместители (группы –СН3, -СН2-СН3, -NO2, -SO3, -Вr и т.д.), они по-разному будут влиять на реакционную способность ароматического кольца в реакциях замещения. По своему действию на реакционную способность бензола все заместители делятся на две группы. Заместители I рода. Это -СН3, -СН2-СН3, -Сl, -Вr, -I, -ОН, -NH2. Эти заместители облегчают введение следующего электрофильного заместителя в ароматическое кольцо и направляют его в орто- или пара-положение. Например, толуол нитруется легче, чем бензол. Нитрогруппа при этом встает в орто- или пара-положение по отношению к группе –СН3 и в результате образуется смесь орто- (I) и паранитротолуолов (II).
Заместители II рода. Это группы –NО2, -SO3H, -CHO, -СООН. Они затрудняют введение следующего электрофильного заместителя в ароматическое кольцо и направляют его в мета-положение по отношению к имеющемуся в кольце заместителю. Например, нитробензол нитруется труднее, чем бензол (необходимы более жесткие условия), и новая нитрогруппа (-NО2) встает в мета-положение по отношению к имеющейся в кольце нитрогруппе.
4. Бензольное кольцо устойчиво к воздействию температуры. Бензол при температурах крекинга (450-500°С) не расщепляется, а в основном конденсируется с образованием кокса. 5. Бензольное кольцо также устойчиво к действию окислителей. При действии сильных окислителей гомологи бензола окисляются по боковым цепям с образованием карбоновой кислоты (чаще всего бензойной).
Сам бензол подвергается окислению только в специфических условиях - при окислении кислородом воздуха при высокой температуре в присутствии оксида ванадия (V).
|