Примеры решения задач. 1. Определить соединения, в которых степень окисления хрома равна +3.
1. Определить соединения, в которых степень окисления хрома равна +3. Решение: Алгебраическая сумма степеней окисления отдельных атомов, образующих молекулу, с учетом стехиометрических индексов равна нулю.
а) Na2+1 Cr2Х O7-2 б) CrХ(О-2Н+)3- (+1)∙2+х∙2+(-2)∙7 = 0 х + 3(-2 + 1) = 0 х= 6 х = 3
в) Cr2ХO3-2 K2+CrХО4-2 х·2+3(-2)=0 2(+1)+4(-2) +х = 0 х = 3 Х = 6 Ответ: б) Cr(ОН)3, в) Cr2O3 2. Определить полуреакции, которым соответствуют процессы восстановления: в) Mn0 → Mn+2 г) Mn+4 → Mn+2 Решение: а) Mn+2 – 5ē = Mn+7 процесс окисления г) Mn+4 + 2ē = Mn+2 процесс восстановления Ответ: б) Mn+7 + 3ē = Mn+4, г) Mn+4 + 2ē = Mn+2.
3. Из предложенных пар выбрать пару веществ, которые способны выполнять функцию только окислителей. а) CO; O2 в) HNO3; KMnO4 б) SO2; H2S г) H2SO3; O3. Решение: Определяем степень окисления элементов в указанных веществах: а) б) Функцию только окислителя способен выполнять элемент, имеющий высшую положительную степень окисления (соответствует номеру группы, в которой находится этот химический элемент). Ответ: в) HNO3; KMnO4
4. Из предложенных пар выбрать пару веществ, которые способны выполнять функцию только восстановителей. а) K; O2 в) C; FeCl3 б) Na; H2S г) NH3; O3. Решение: Определяем степень окисления элементов а) б) Функцию восстановителя способен выполнять элемент, имеющий низшую отрицательную степень окисления или металл. Ответ: б) Na; H2S
5.Уравнять реакции: а) Ca + HNO3 → Ca(NO3)2 + N2O + H2O б) Se + HNO3 → H2SeO4 + NO2 + H2O в) Si + H2SO4 → H2SiO3 + SO2 + H2O г) Ba + H2SO4 → BaSO4 + H2S + H2O
Решение:
|

 ;
;  в)
в)  ;
; 
 ;
;  г)
г)  ;
; 
 ;
;  ;
; 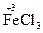
 ;
; 
 ;
; 



