Диффузия в газах
Диффузия – обусловленное тепловым движением самопроизвольное взаимное проникновение и перемешивание частиц соприкасающихся газов, жидкостей или твердых тел. Диффузия происходит в направлении уменьшения концентрации вещества (т.е. оттуда, где вещества больше, туда, где его меньше). Процесс диффузии может происходить между различными агрегатными состояниями вещества. Например, в полупроводниковой технологии p-n-переходы создаются диффузией примеси, находящейся в газообразном или жидком состоянии, в твердый полупроводник (нагретый до 1000 – 1300 °С). Установлено, что поток молекул, прошедших за время dt через площадку dS, перпендикулярную направлению переноса вещества, определяется законом Фика:
Умножив обе части формулы (26) на массу одной молекулы, получим выражение для потока массы и градиента плотности:
Из-за теплового движения молекулы будут переходить через площадку dS как слева направо, так и справа налево. Однако, из-за раз-ности концентраций возникает диффузионный поток в направлении оси z. За время dt через площадку dS пройдут N молекул: N = N' - N''. (28) Поскольку тепловое движение хаотическое, тепловые скорости молекул равномерно распределены по трем осям x, y, z. Причем из 1/3 всех молекул, которые движутся вдоль оси z, одна половина движется в положительном направлении оси z, а другая половина – в отрицательном. Таким образом, в положительном направлении оси z движется 1/6 часть молекул. За время dt до площадки dS долетят все движущиеся по направлению к ней молекулы, заключенные в элементе объема с основанием dS и высотой áυñ dt. Умножив эти элементы объема на концентрации молекул с одной и другой стороны площадки (n' и n''), получим количество молекул N' и N'', прошедших через площадку dS в противоположных направлениях:
Подставив уравнения (29) в формулу (28), получим:
Очевидно, что через площадку dS будут пролетать лишь те молекулы, которые испытали последнее соударение на различных расстояниях от dS. Значит, n' и n'' – это концентрации молекул, которые существуют на расстоянии длины свободного пробега l по обе стороны от площадки. Так как dn/dz – есть разность концентраций, приходящихся на единицу длины, то на расстоянии 2l разность концентраций равна
Подставив уравнение (31) в формулу (30), окончательно получим:
Сравнивая формулы (26) и (32), находим коэффициент диффузии:
Полученная формула (33) определяет коэффициент самодиффузии, т.е. диффузию молекул газа в среде того же газа. Когда молекулы обеих компонент смеси неодинаковы по массе и эффективному сечению, коэффициент диффузии определяется более сложным выражением. Например, в смеси водорода и углекислого газа водород должен диффундировать быстрее, чем углекислый газ, так как средняя скорость молекул водорода почти в 5 раз выше, чем у углекислого газа, кроме того, l(H2) > l(СО2). Это значит, что объем водорода, переносимого в одном направлении, больше объема углекислого газа, переносимого в противоположном направлении. При этом неизбежно возникает разность давлений, которая влияет на процесс диффузии.
|

 , (26)
, (26)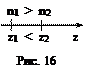 где dN – количество частиц (молекул); D – коэффициент диффузии; dn/dz – градиент концентрации в направлении оси z. Знак "минус" в формуле (26) обусловлен тем, что поток молекул направлен в сторону убывания концентрации. Знак "минус" компенсирует отрицательный знак градиента (рис. 16):
где dN – количество частиц (молекул); D – коэффициент диффузии; dn/dz – градиент концентрации в направлении оси z. Знак "минус" в формуле (26) обусловлен тем, что поток молекул направлен в сторону убывания концентрации. Знак "минус" компенсирует отрицательный знак градиента (рис. 16):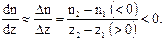
 . (27)
. (27)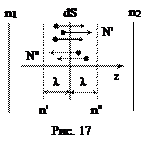 Рассмотрим процесс диффузии в газах и найдем коэффициент диффузии. Пусть диффузия – стационарная, т.е. градиент концентрации (или плотности) является постоянным и не зависящим от времени. Рассмотрим площадку dS, перпендикулярную оси z (рис. 17). Пусть n1 > n2.
Рассмотрим процесс диффузии в газах и найдем коэффициент диффузии. Пусть диффузия – стационарная, т.е. градиент концентрации (или плотности) является постоянным и не зависящим от времени. Рассмотрим площадку dS, перпендикулярную оси z (рис. 17). Пусть n1 > n2.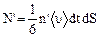 ,
,  . (29)
. (29) (30)
(30) (31)
(31) (32)
(32)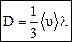 . (33)
. (33)


