Лабораторна робота № 29
ВИЗНАЧЕННЯ ЗМІНИ ЕНТРОПІЇ В ПРОЦЕСІ НАГРІВАННЯ І ПЛАВЛЕННЯ ОЛОВА
Мета роботи:визначення зміни ентропії за фазового переходу першого роду на прикладі плавлення олова. Обладнання:експериментальна установка ФПТ 1-11. Теоретичні відомості Фазовий перехід першого роду - це фазове перетворення, яке супроводжується поглинанням або виділенням деякої кількості прихованої теплоти та зміною питомого об'єму речовини; температура переходу залишається сталою і залежить від тиску. Отже, для розплавлення деякої маси т речовини, що знаходиться при температурі плавлення Т П, необхідно витратити кількість теплоти
Q П = λ · m, (29.1)
де λ - питома теплота плавлення даної речовини. Ентропією зветься така функція стану термодинамічної системи, диференціал якої dS в оборотному процесі дорівнює відношенню нескінченно малої кількості теплоти δQ наданої системі, до термодинамічної температури Т системи:
Ентропія завжди визначається з точністю до сталої величини, тому зміст має лише її зміна при переході системи зі стану 1до стану 2:
Процес плавлення олова проходить за сталої температури Т=ТП і, отже, є ізотермічним. Зміну ентропії у такому процесі можна знайти за формулою (29.3):
З виразу (29.3) випливає, що зміну ентропії при нагріванні і плавленні олова можна визначити як суму зміни ентропії при нагріванні його від початкової температури Т Кдо температури плавлення Т П та при плавленні олова:
Враховуючи, що δQ H = c ·m·dt, і беручи до уваги формулу (29.1), отримуємо
або
де с і λ - питома теплоємність та питома теплота плавлення олова. Формула (29.4) може бути використана для експериментального визначення зміни ентропії при нагріванні та плавленні олова після вимірювання значень температур Т Кі Т П.
|

 . (29.2)
. (29.2)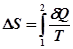 . (29.3)
. (29.3)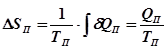 .
. .
.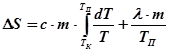
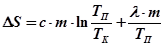 , (29.4)
, (29.4)


