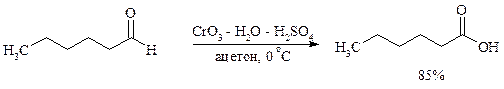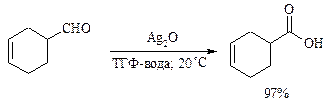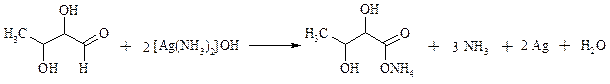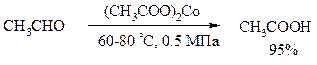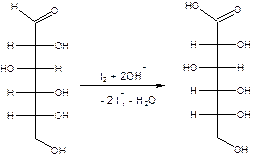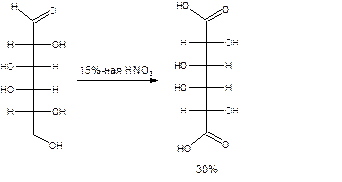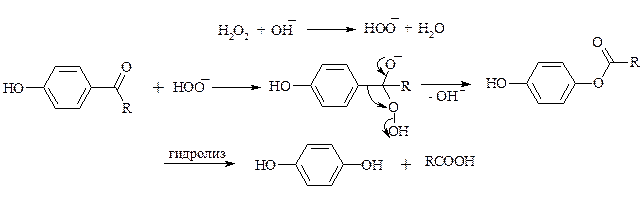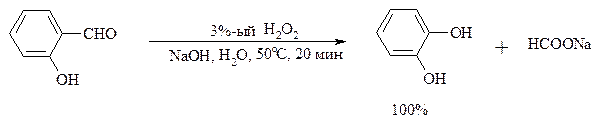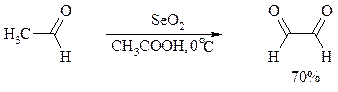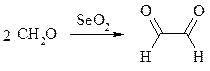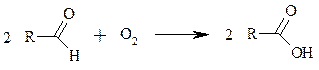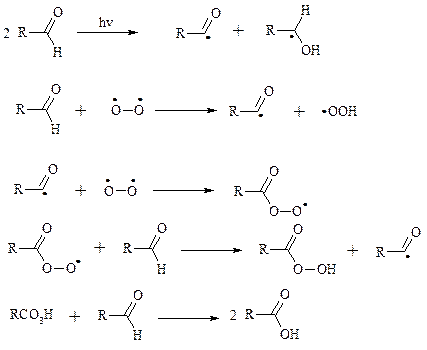ОКИСЛЕНИЕ АЛЬДЕГИДОВ
Окисление альдегидов протекает значительно легче, чем окисление спиртов. Превращение альдегидов в карбоновые кислоты можно осуществить действием многих окислителей: HNO3, H2O2, KMnO4, NaClO2, Ag2O, щелочным раствором иода, соединениями хрома (VI). Наилучшие результаты дает обычно реагент Джонса. В этом случае окисление проводится при 0-20°С в течение короткого промежутка времени с выходами больше 80%.
Однако реагент Джонса не обладает высокой избирательностью по отношению к другим функциональным группам, а кислая среда иногда приводит к изомеризации или деструкции. В таких случаях идеальным селективным окислителем является водно-спиртовой раствор оксида серебра или раствор AgNO3 в водном аммиаке (реагент Толленса). Этот реагент не затрагивает кратные углерод-углеродные связи, гидроксильную группу спиртов и ряд других функциональных групп:
Окисление уксусного альдегида в промышленности осуществляют действием кислорода в присутствии солей кобальта или марганца в качестве катализатора:
В химии углеводов для селективного окисления альдегидных групп применяется щелочной раствор иода. Так из D-глюкозы образуется D-глюконовая кислота:
Применяя разбавленную азотную кислоту, осуществляют окисление альдегидной группы, не затрагивая присутствующей в молекуле вторичной спиртовой группы, однако первичная спиртовая группа при этом окисляется в карбоксильную:
При обработке щелочным раствором пероксида водорода ароматических альдегидов (а также кетонов), содержащих в орто- или пара- положении NH2- или OH-группу, образуются соответственно аминофенолы или двухатомные фенолы (реакция Дакина):
Под действием SeO2 альдегиды окисляются в a-дикарбонильные соединения:
Интересно отметить, что при окислении диоксидом селена формальдегида образуется глиоксаль:
Альдегиды медленно окисляются кислородом воздуха при комнатной температуре до карбоновых кислот (аутоокисление альдегидов).
Эта реакция ускоряется при облучении или ионами Fe(II) и представляет собой цепной радикальный процесс:
|