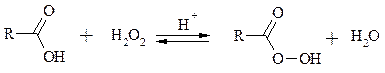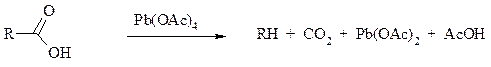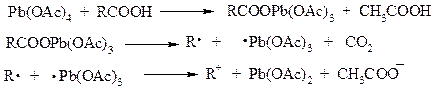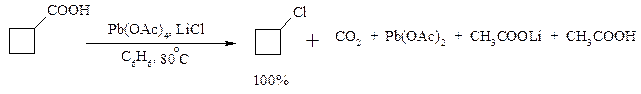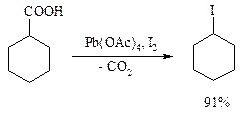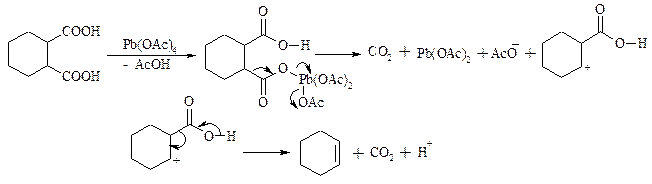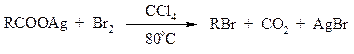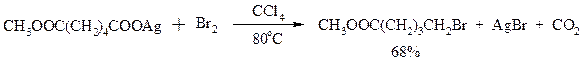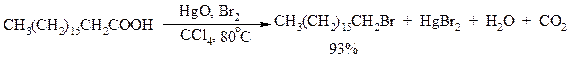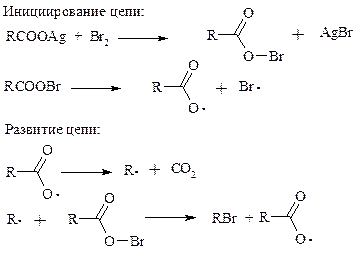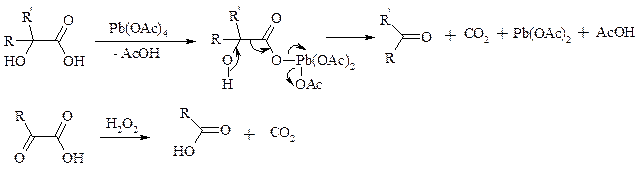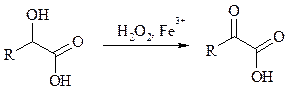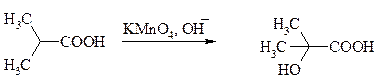ОКИСЛЕНИЕ КАРБОНОВЫХ КИСЛОТ
При действии пероксида водорода в присутствии кислотного катализатора на карбоновые кислоты образуются перкислоты (надкислоты):
Наиболее распространенным катализатором в случае алифатических карбоновых кислот является концентрированная H2SO4. Реакция обратима, и равновесие можно сместить вправо, удаляя воду или применяя избыток реагента. Для субстратов с ароматическими группами R наилучшим катализатором является метансульфокислота, которая используется и как растворитель. Карбоновые кислоты подвергаются окислительному декарбоксилированию под действием тетраацетата свинца и в качестве продуктов в зависимости от условий получаются алканы, алкены или эфиры уксусной кислоты:
Для данной реакции предполагается следующий механизм:
Алканы образуются за счет отрыва атома водорода от молекул растворителя радикалом R, а алкен и сложный эфир из карбокатиона соответственно за счет отщепления протона или захвата ацетат-иона. Введение в реакционную смесь галогенид-иона практически нацело подавляет оба процесса и приводит к образованию алкилгалогенидов.
В присутствии иода и тетраацетата свинца карбоновые кислоты превращаются в соответствующие иодиды:
Из 1,2-дикарбоновых кислот под действием тетраацетата свинца образуются алкены:
Другим примером окислительного декарбоксилирования может служить окисление серебряных солей карбоновых кислот бромом в CCl4 с образованием алкилбромидов (реакция Хунсдиккера – Бородина):
Для успешного проведения реакции требуется применять тщательно высушенные серебряные соли карбоновых кислот, и выход алкилбромида колеблется в широких пределах в зависимости от степени очистки и обезвоживания соли. Этого недостатка лишена модификация с использованием ртутных солей, причем ртутную соль не выделяют индивидуально, а смесь карбоновой кислоты, оксида ртути (II) и брома нагревают в индифферентном растворителе. Этот метод приводит, как правило, к более высоким и воспроизводимым выходам.
Для реакции Хунсдиккера – Бородина установлен цепной радикальный механизм. Образующийся в первой стадии ацилгипобромит подвергается гомолитическому расщеплению с образованием карбоксильного радикала и атома брома. Карбоксильный радикал теряет CO2 и превращается в алкильный радикал, который затем регенерирует цепь, отщепляя атом брома от ацилгипобромита.
a-Гидрокси- и a-кетокислоты не расщепляются под действием HIO4, но эта реакция идет с тетраацетатом свинца, H2O2 в щелочной среде и другими реагентами. Такие реакции представляют собой окислительное декарбоксилирование. Из a-гидроксикислот получаются альдегиды или кетоны, а из a-кетокислот – карбоновые кислоты:
В то же время при использовании пероксида водорода в присутствии Fe(III) удается окислить гидроксильную группу в a-гидроксикислотах в карбонильную с сохранением карбоксильной:
Окислить алифатические карбоновые кислоты в α-гидроксикислоты удается в том случае, если кислота содержит третичный атом углерода в α-положении к карбоксильной группе. В качестве окислителя применяют щелочной раствор KMnO4.
|