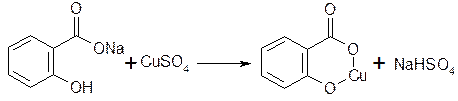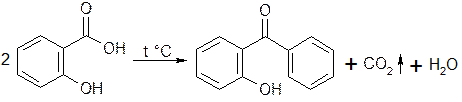Получение
Натрия бензоат и натрия салицилат получают, выпаривая досуха раствор соответствующей кислоты (бензойной или салициловой), нейтрализованной эквивалентным количеством карбоната или гидрокарбоната натрия:
Соли перекристаллизовывают из спирта.
Реакции подлинности. 1. ГФ Х. Бензойную кислоту и ее соли определяют по реакции комплексообразования с FeCl3.
1.1. Кислоту нейтрализуют щелочью (по индикатору рН≈7). В кислой среде осадок растворяется, в щелочной среде выпадает бурый осадок гидроксида железа (III).
1.2. С хлоридом железа (III) образуется комплексная соль: 6 C6H5COONa + 2FeCl3 + 10H2O → → (C6H5COO)3Fe·Fe(OH)3·7H2O↓ + 3 C6H5COOH + 6 NaCl желтовато-розовый цвет
2. Реакция образования салицилатного комплекса. 2.1. Для бензойной кислоты и бензоата натрия.
2.2. Салициловую кислоту доказывают по фиолетовому окрашиванию комплекса с хлоридом железа (III).
моносалицилат железа фиолетовый цвет рН=2-3
Для салициловой кислоты и ее соли:
Моносалицилат дисалицилат трисалицилат рН=2-3 рН=3-8 рН=8-10 фиолетовый красный желтый При добавлении минеральных кислот указанные комплексы разрушаются, окраска исчезает и выпадает белый осадок салициловой кислоты. В присутствии СН3СООН окраска сохраняется. Соли кислот вступают в реакцию с другими солями тяжелых металлов.
зеленый цвет
3. Реакция декарбоксилирования. 3.1. При нагревании выделяется фенол, который определяют по запаху:
запах фенола
3.2. С концентрированной серной кислотой
СО2+ Са(ОН)2 → СаСО3↓+Н2О помутнение
4. Реакция конденсации с реактивом Марки.
5. Реакция этерификации с этанолом.
C6H5COOН + C2H5OH C6H5COOC2H5 + Н2О
Тпл=122-124,5˚С для бензойной кислоты, Тпл=158-161˚С для салициловой кислоты.
|