Опыт № 2. Пиридин и его свойства
2. 1. Растворимость пиридина в воде и его основные свойства Пиридин быстро и в любых соотношениях растворяется в воде. К 1 мл пиридина приливают 5 мл воды. Каплю полученного раствора наносят на красную лакмусовую бумагу. Водный раствор пиридина проявляет слабые основные свойства:
_ + Н2О → ОН.
Н
К капле пиридина осторожно прибавляют концентрированную серную кислоту. Реакционная смесь сильно разогревается, и выпадает белый осадок. К полученному осадку приливают воду. Наблюдают его растворение. 2.2. Образование солей пиридина В две пробирки наливают по 1 мл 2 %-х растворов хлорида железа (III) и сульфата меди (II) и добавляют по 1–2 капли раствора пиридина, полученного в предыдущем опыте. В пробирке с хлоридом железа (III) выпадает осадок бурого цвета:
3 ОН + FеCℓ 3 → 3 Cℓ + Fе(ОН)3↓.
Н Н
Н Н хлорид пиридиния
В пробирке с сульфатом меди (II) сначала выпадает голубой осадок гидроксида меди (II):
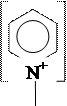
2 ОН + СuSО4 → SО4 + Сu(ОН)2↓.
2 Н Н сульфат пиридиния В избытке пиридина осадок гидроксида меди (II) быстро растворяется с образованием комплексной соли ярко-синего цвета. 2.3. Образование пикрата пиридиния К 1 мл насыщенного раствора пикриновой кислоты приливают 5–10 капель раствора пиридина. При встряхивании образуются игольчатые кристаллы пикрата пиридиния. Эта реакция используется для обнаружения пиридина. 2.4. Отношение пиридина к окислению В пробирку поместите по 3 капли водного раствора пиридина, 2 %-го раствора перманганата калия и 5 %-го раствора карбоната натрия. Содержимое пробирки тщательно встряхните и нагрейте до кипения. Происходит ли обесцвечивание раствора перманганата калия? Задания: 1. Указать, почему водный раствор пиридина изменяет окраску красного лакмуса. 2. Какие свойства пиридина проявляются в реакции с пиридиновой кислотой? Написать схему образования пикрата пиридина. 3. Объяснить устойчивость пиридина к окислению. 4. Объяснить, каким критериям ароматичности удовлетворяет молекула пиридина.
Результаты исследований занести в таблицу 1 (см. с. 13).
Контрольные вопросы
1. Докажите ароматический характер и наличие кислотно-основных свойств с учетом электронного строения гетероатомов пиридина, пиримидина, пурина, хинолина. Написать схему реакции получения метилпиридиний йодида и реакцию взаимодействия его с гидрид-ионом. Объясните механизм реакции N–метилирования. 2. Почему пяти- (пиррол, тиофен, имидазол) и шестичленные (пиридин) гетероциклы способны вступать в реакции электрофильного замещения? Написать уравнение реакции названных гетероциклов. 3. Приведите схему получения пурина из мочевой кислоты.
|



 _ 2-
_ 2-


