Другий і третій закони термодинаміки
Перший закон термодинаміки, який встановив кількісний зв’язок між теплотою, роботою і внутрішньою енергією системи, не дозволяє визначити напрямок протікання термодинамічних процесів. Другий закон термодинаміки якраз вказує на напрямок теплових процесів, що відбуваються в природі. Згідно із Клаузіусом, який дав одне з перших формулювань другого закону, теплота ніколи не може переходити сама собою від тіл з нижчою температурою до тіл з вищою температурою. Це означає, що для такого переходу теплоти потрібна затрата роботи зовнішнього джерела, що здійснюється в холодильній машині. Фізичний зміст другого закону найбільш зрозуміло розкривається у формулюванні Планка: неможливо побудувати таку періодично діючу теплову машину, яка, отримавши ззовні деяку кількість теплоти при довільній температурі, цілком перетворювала би її в механічну роботу і при цьому поверталась би точно у вихідний стан. Отже, в довільній тепловій машині перетворюється в роботу лише частина отриманої від нагрівника кількість теплоти, тобто
завжди значно менший від одиниці. Із формули ККД теплової машини, що працює за циклом Карно,
випливає, що Вираз для ККД теплової машини, яка працює за циклом Карно, теж є одним з формулювань другого закону: коефіцієнт корисної дії ідеальної теплової машини визначається лише температурами нагрівника i холодильника. Кельвін сформулював другий закон термодинаміки в такому вигляді: неможливо побудувати теплову машину, яка виконувала би роботу за рахунок теплоти найбільш холодного з тіл, що є в системі. Такою машиною могла би бути машина, яка перетворювала б в роботу теплоту води в океані. Якби відніманням теплоти i перетворенням її в роботу вдалось би понизити температуру всієї океанської води лише на Вічний двигун першого роду протирічить закону збереження енергії; вічний двигун другого роду не протирічить закону збереження енергії, але він протирічить другому закону термодинаміки. Другий закон термодинаміки вказує на необоротність процесу перетворення однієї форми передачі енергії – роботи – у другу форму передачі енергії – теплоту. Він стверджує, що процес переходу впорядкованого руху тіла як цілого в неупорядкований рух його частинок є необоротним. Упорядкований рух може переходити в неупорядкований без будь-яких додаткових процесів, як це відбувається, наприклад, при внутрішньому терті. Перехід же невпорядкованого руху частинок у впорядкований рух тіл можливий лише при умові, що він супроводжується будь-яким компенсуючим процесом. Оскільки реальні процеси не оборотні, то всі процеси в замкненій системі ведуть до збільшення її ентропії. Цей принцип лежить в основі формулювання другого закону термодинаміки: можливі лише такі процеси, що відбуваються в макроскопічній замкненій системі, які ведуть до збільшення її ентропії. Формула Больцмана дозволяє дати таке статистичне тлумачення другому закону термодинаміки: термодинамічна ймовірність стану ізольованої системи при всіх процесах, що в ній відбуваються не може зменшуватися. Отже, при всякому процесі, що відбувається в ізольованій системі, зміна термодинамічної ймовірності її стану
У випадку оборотного процесу Отже, другий закон термодинаміки є законом статистичним, тобто можливі процеси в ізольованій системі, які приводять не до збільшення, а до зменшення ентропії, не лише для явищ мікросвіту, але і для звичайних макроскопічних явищ; правда, ймовірність таких процесів в наших земних умовах дуже мала. З багатьох дослідів, що проводились при низьких температурах, можна зробити висновок, який сформулював Нернст у такому вигляді: при абсолютному нулі температури будь-які зміни стану відбуваються без зміни ентропії:
Тут мова йде не про абсолютне значення ентропії, а про її зміну. Інтегруючи вираз для ентропії, ми не можемо визначити сталої інтегрування. Згідно з Планком, ентропія будь-якого конденсованого тіла зі зменшенням його температури до абсолютного нуля прямує до певного сталого значення незалежно від індивідуальних властивостей тіла. Або можна стверджувати, що ентропія всіх тіл при абсолютному нулеві набирає однакового значення – вона дорівнює нулю. Отже теорему Нернста – третій закон термодинаміки можна сформулювати так: при абсолютному нулі ентропія дорівнює нулю:
Третій закон термодинаміки заперечує можливість досягнення абсолютного нуля. Справді, всі процеси, які протікають з теплопередачею, супроводжуються зміною ентропії. Це означає, що при Отже, не можна створити машину, яка здатна взяти всю теплоту від тіла, тобто охолодити його до абсолютного нуля.
|

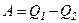 . Теплота
. Теплота  не використовується в машині і розсіюється в навколишньому середовищі. Величина
не використовується в машині і розсіюється в навколишньому середовищі. Величина 
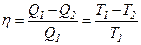
 К, то можна було би приводити в рух усі машини i верстати на земній кулі упродовж 1500 років. Така машина була би еквівалентна вічному двигуну, тому її називають вічним двигуном другого роду, на відміну від вічного двигуна першого роду, який повинен створювати роботу з нічого, без затрати енергії.
К, то можна було би приводити в рух усі машини i верстати на земній кулі упродовж 1500 років. Така машина була би еквівалентна вічному двигуну, тому її називають вічним двигуном другого роду, на відміну від вічного двигуна першого роду, який повинен створювати роботу з нічого, без затрати енергії.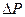 додатна або дорівнює нулю:
додатна або дорівнює нулю:
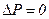 , тобто термодинамічна ймовірність Р не змінюється, а у випадку необоротного процесу
, тобто термодинамічна ймовірність Р не змінюється, а у випадку необоротного процесу 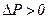 і Р зростає.
і Р зростає.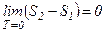 .
.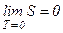 .
.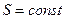 процес з теплопередачею не
процес з теплопередачею не 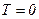 система більше не віддає теплоти, тобто не охолоджується.
система більше не віддає теплоти, тобто не охолоджується.


