Методы качественного и количественного анализа галогенпроизводных углеводородов
Методы качественного и количественного анализа галогенпроизводных углеводородов сводятся чаще всего к определению галогена. Галоген в молекулах органических лекарственных веществ ковалентно связан с атомом углерода, в связи с чем для его определения необходимо предварительно минерализовать лекарственное средство. В зависимости от природы галогена, а также от строения органической молекулы прочность ковалентной связи галоген-углерод неодинакова, поэтому для минерализации применяют различные, соответствующие этой прочности методы. Для минерализации галогенов в органических соединениях широко применяются методы восстановления водородом в момент выделения. Существует несколько вариантов метода восстановления, в зависимости от способа получения водорода: 1) действием металлического натрия на спирт; 2) цинковой пыли в кислой среде; 3) цинковой пыли в щелочной среде. Из этих методов наиболее удобным и часто применяемым является восстановление цинком в щелочной среде, так как в этом случае образуется нелетучие галогениды. Хлористый этил, хлороформ качественно и количественно определяется взаимодействием с серебра нитратом после переведения хлора в ионное состояние при взаимодействии со щелочами:
В галотане (фторотане) для переведения фтора в ионогенное состояние лекарственное средство сплавляют с металлическим натрием, при этом хлор и бром также переходят в ионное состояние. Фторид ионы открывают смесью циркония нитрата и ализаринового красного, Нагреванием с избытком серебра нитрата в азотнокислой среде определяют количественно йодоформ, предохраняя его от действия света. Избыток серебра нитрата оттитровывают раствором аммония тиоционата с индикатором железа (III) аммония сульфатом.
Окислительный метод количественной оценки галоген-углеводородов по содержанию, например ковалентно связанного йода (тиреоидин), основывается на разрушении субстанции пероксидом водорода в смеси с концентрированной серной кислотой. При этом образуются йодиды и частично йодаты. Йодиды окисляются до йодатов 5% раствором калия перманганата:
Избыток калия перманганата удаляют натрия нитритом:
Избыток нитрита разрушают с помощью мочевины:
После удаления окислителей в растворах остается только йодноватая кислота в количестве, эквивалентном содержанию йода в навеске тиреоидина. Её определяют методом йодометрии:
Международная фармакопея 3 издания и фармакопеи ряда стран включили метод сжигания органических веществ в атмосфере кислорода для определения галогенов. Сущность метода состоит в том, что органическое вещество сжигают в колбе, наполненной кислородом. Образующиеся продукты сгорания (галогенводородные кислоты) поглощаются раствором щелочи. Хлориды и бромид определяют меркуриметрически. При анализе йодпроизводных йодид окисляют до йодатов, а после прибавления калия йодида выделившийся йод титруют тиосульфатом. Спирты – углеводороды, в которых один или несколько атомов водорода замещены гидроксилом. Введение гидроксила в молекулу углеводорода оказывает влияние на физико-химические и биологические свойства: повышает растворимость вещества в воде; с увеличением числа гидроксильных групп снижается токсичность, появляется сладкий вкус (глицерин, маннит, сорбит). Спирты реагируют со щелочными металлами с выделением водорода:
образующийся алкоголят подвергается гидролизу:
Спирты проявляют восстановительные свойства, окисляясь под действием сильных окислителей (KMnO4, K2Cr2O7) до альдегидов и далее до кислот. Вследствие того, что раствор калия перманганата при этом изменяет окраску, данная реакция может быть использована для идентификации спиртов:
Вторичные спирты окисляются до кетонов:
Образование сложных эфиров при взаимодействии с неорганическими и органическими кислотами используется для синтеза лекарственных средств из группы сложных эфиров, а также для идентификации спиртов (при условии, что образующийся эфир имеет характерный запах):
Альдегиды и кетоны характеризуются наличием в их структуре карбонильной группы >С=О, которая у альдегидов связана с радикалом (алифатическим, ароматическим, гетероциклическим) и водородом – В химическом отношении альдегиды являются реакционно-способными соединениями, что обусловлено наличием в их молекуле сильно поляризованной двойной связи (С=О), за счёт которой происходит большинство реакций, характеризующих химические свойства альдегидов. Многие из этих реакций используются для идентификации лекарственных веществ, содержащих в своем составе карбонильную группу, для определения этих веществ в качестве примесей, в количественном анализе. 1. Альдегиды способны легко окислятся, т.е. являются сильными восстановителями. Они подвергаются окислению даже под действием таких слабых окислителей как соли тяжелых металлов до соответствующих кислот. Однако для повышения редокспотенциала пары а) Для идентификации альдегидов используют реакцию с аммиачным раствором нитрата серебра – реакцию "серебряного зеркала" (раствор формальдегида, хлоралгидрат и др.). Реакция протекает при нагревании, в результате ее на стенках пробирки образуется серебряный налёт.
б) При нагревании с меднотартратным комплексом альдегиды окисляются до кислот и выпадает осадок меди (I) оксида:
в) При взаимодействии с калия тетрайодмеркуратом щелочным раствором (реактив Несслера) выпадает темный осадок восстановленной ртути (реакция используется для определения альдегидов как примесей в лекарственных веществах):
2. Для альдегидов типичны реакции присоединения по месту разрыва двойной связи. Присоединение воды приводит к образованию гидратной формы альдегида, что приводит к снижению его токсичности:
К реакциям присоединения относятся взаимодействие альдегидов с фуксинсернистой кислотой (используется для идентификации формальдегида); натрия бисульфитом. Бисульфитные производные альдегидов – кристаллические вещества, что даёт возможность использовать их образование для идентификации альдегидов (по температуре плавления) и их очистке.
3. Характерным свойством альдегидов является их способность конденсироваться как между собой (альдольная конденсация), так и с соединениями, содержащими в своей структуре фенольный гидроксил. Эта реакция характерна для многих веществ, содержащих карбонильную группу.
ГФУ предлагает для идентификации формальдегида его конденсацию с хромотроповой кислотой. Реакция протекает в присутствии концентрированной кислоты серной, при этом образуется продукт конденсации, окрашенный в фиолетовый цвет:
4. Для альдегидов и кетонов характерны реакции замещения, которые являются своеобразным типом реакций конденсации. Реакции замещения с аминами (алифатическими, ароматическими, гетероциклическими) используют как для идентификации альдегидов (часто получают окрашенные соединения, причем окраска может быть специфична для каждого альдегида), так и для количественного определения (оксимный метод). Для идентификации чаще всего используют замещенный гидразин, при этом образуются гидразоны; семикарбазид (семикарбазоны). Все перечисленные соединения имеют определенную температуру плавления.
5. Способность альдегидов к полимеризации, которая может протекать в водном растворе через гидратную форму учитывается при хранении растворов альдегидов. Образующийся полимер является примесью, снижающий фармакологический эффект препарата. Например, примесь параформа в растворе формальдегида, гексаметилентетрамине
В фармакологическом отношении альдегиды проявляют антисептические и наркотические свойства. Альдегидная группа увеличивает токсичность соединений.
|



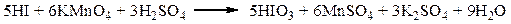



 ,
,
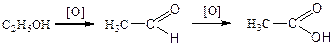

 .
.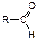 , а у кетонов – с двумя заместителями
, а у кетонов – с двумя заместителями  .
. реакцию необходимо проводить в щелочной среде.
реакцию необходимо проводить в щелочной среде.