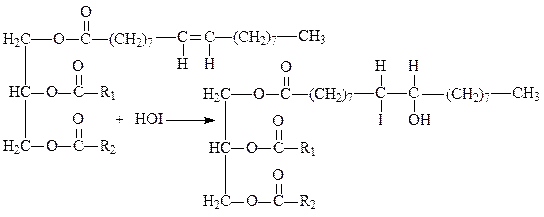Работа 10.1. Определение йодного числа молочного жира
Метод основан на способности непредельных жирных кислот молочного жира присоединять йод. В триацилглицеринах молочного жира обнаружено более 140 жирных кислот с числом атомов углерода от 4 до 26. Однако только 10...12 кислот с четным числом атомов углерода от 4 до 18 встречаются в количестве от 1 до 5% каждая. Их называют главными. Остальные кислоты получили названия минорных. Из главных кислот в составе молочного жира преобладают предельные, на их долю в среднем приходится 65% всей массы жирных кислот. Среди непредельных примерно 30% составляет олеиновая кислота. Количество биологически важных полиненасыщенных кислот — линолевой, линоленовой и арахидоновой, невелико и составляет 3…5 % всей массы жирных кислот. Для характеристики степени непредельности жирных кислот молочного жира используют йодное число. Таблица 4.1 Физико-химические свойства молочного жира, животных жиров и растительных масел
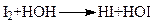
Количественно йодное число выражается в граммах йода, присоединяющегося к 100 граммам жира. Йодное число молочного жира зависит от кормовых рационов, стадии лактации, породы животного и других факторов. Среднее значение йодного числа лежит в пределах от 28 до 45 единиц. Зимой при стойловом содержании скота значения йодных чисел невысоки (менее 33 единиц). Весной с началом пастбищного периода они возрастают, достигая максимума летом (до 39 единиц и выше). Осенью в связи с переходом животных с пастбищного содержания на стойловое йодные числа уменьшаются и зимой имеют минимальные значения (от 28 единиц). В течение года колебания йодного числа в пределах одной области обычно не превышают 6...8 единиц. Существует тесная связь между йодным числом, числом рефракции (с понятием «число рефракции» - и методами его определения можно ознакомиться в работе «Определение показателя преломления молочного жира») и температурой плавления молочного жира. Так, йодное число меньше 33 единиц характеризует высокоплавкий жир (температура плавления около 32°С) и наоборот. С увеличением йодного числа улучшается способность молочного жира к связыванию влаги, поэтому летом легче, чем зимой, вырабатывать масло с повышенной массовой долей влаги. От йодного числа зависят многие технологические процессы выработки масла высокого качества: продолжительность физического созревания и интенсивность сбивания сливок, продолжительность обработки масла, режимы преобразования высокожирных сливок и другие. По мере хранения молочного жира количество непредельных жирных кислот понижается благодаря их высокой реакционной способности. Это приводит к уменьшению значения йодного числа и может служить косвенной характеристикой степени свежести жира. Методы определения йодного числа основаны на способности непредельных жирных кислот присоединять йод. Реакции, характеризующие процесс, описываются следующими уравнениями:
В обычных условиях йод практически не реагирует с водой, но в присутствии веществ, поглощающих йодноватистую кислоту, равновесие реакции сдвигается вправо:
Избыток йода оттитровывают тиосульфатом натрия:
Реактивы и материалы: ü Колба коническая с притертой пробкой вместимостью 400 см3 ü Весы лабораторные 2 класса точности с ценой поверочного деления 0,001 г ü Бюретки вместимостью 25 и 50 см3 и ценой деления 0,1 см3 ü Баня водяная для колб ü Электроплитка ü Цилиндр вместимостью 200 см3 ü Секундомер ü Встряхивалка ü Молочный жир ü Спиртовой раствор йода (Сэ = 0,2 моль/дм3) ü 1%-ный раствор крахмала ü Раствор тиосульфата натрия ü Дистиллированная вода
Методика проведения анализа: Берут две конические колбы вместимостью по 400 см3 с притертыми пробками. В одну отвешивают 0,20...0,30 г ± 0,01г расплавленного и профильтрованного жира (опытная проба), другую оставляют пустой (контрольная проба). В обе колбы из бюретки добавляют по 20 см3 96%-ного этанола. Опытную пробу нагревают на водяной бане с температурой 50...60 °С до получения однородной эмульсии. Затем в обе колбы из бюретки вносят по 25 см3 спиртового раствора йода (Сэ = 0,2 моль/дм3) и цилиндром - по 200 см3 дистиллированной воды, содержимое перемешивают. Колбы закрывают пробками и выдерживают при комнатной температуре в темном месте в течение 15 мин. Далее реакционную смесь в каждой колбе быстро (чтобы максимально связать избыток йода) титруют из бюретки раствором тиосульфата натрия (Сэ = 0,1 моль/дм3) до желтого окрашивания, после чего добавляют 1 см3 1%-ного раствора крахмала. Смесь приобретает буро-фиолетовое окрашивание. Содержимое колбы вновь титруют раствором тиосульфата натрия, добавляя его по каплям до обесцвечивания. В расчете используют весь объем раствора тиосульфата натрия, израсходованного на титрование каждой пробы.
Обработка результатов: Йодное число (в единицах, ед.) вычисляют по формуле:
К = К = ((Vk-Vo) · 0.01269 ·100)/ m где К— йодное число, ед. (1 ед, соответствует 1 г йода, присоединяющегося к 100 г жира); V к— объем раствора тиосульфата натрия, израсходованного на титрование контрольной пробы, см3; V o — объем раствора тиосульфата натрия, израсходованного на титрование опытной пробы, см3; 0,01269 — масса йода, соответствующая 1 см3 раствора тиосульфата натрия с эквивалентной концентрацией 0,1 моль/дм3, г; т — масса жира, г; 100 — коэффициент пересчета на 100 г жира.
|