Статистичний і термодинамічний методи дослідження. Тепловий рух. Основні поняття
Молекулярна фізика вивчає фізичні властивості і агрегатні стани тіл в залежності від їх молекулярної будови, сил взаємодії між складовими частинками тіл і характеру теплового руху цих частинок. Термодинаміка або наука про теплоту теж вивчає властивості тіл і зміни станів речовини. Названі розділи фізики відрізняються лише використовуваними методами дослідження, що взаємно доповнюють один одного. Молекулярно-кінетичний або статистичний метод опису стану системи базується на положенні про молекулярну будову речовини та безперервний тепловий рух молекул, використовує закономірності великого числа частинок, з яких складається розглядувана система. При цьому рухом окремих молекул не цікавляться, а оперують параметрами стану системи, що спостерігаються на досліді: тиском (р), температурою (Т) і об’ємом (V). Зв’язок між цими параметрами для заданої маси речовини називається рівнянням стану системи. Загальна форма запису рівняння стану Термодинамічний метод полягає у вивченні властивостей системи взаємодіючих тіл шляхом аналізу кількісних співвідношень та умов перетворень енергії. При цьому не використовуються ніякі уявлення про внутрішню будову і характер руху мікрочастинок. Вивчаються макроскопічні характеристики системи на основі кількох експериментально встановлених законів – начал термодинаміки. Термодинамічна система – це сукупність макрооб’єктів (тіл і полів), що обмінюються енергією у формі роботи і тепла як між собою, так із зовнішнім середовищем. Рівноважним станом системи називають такий стан, при якому всі параметри стану мають певні значення, постійні при незмінних зовнішніх умовах. Перехід системи з одного стану в інший називається процесом. Якщо такий перехід дуже повільний (в ідеальному випадку – безмежно повільний), то процес буде послідовністю рівноважних станів. Ідеальним газом називається система невзаємодіючих матеріальних точок, що при зіткненні ведуть себе як абсолютно пружні кульки. Практично – це газ, у котрого розміри молекул значно менші від середньої міжмолекулярної відстані. Моль – це така кількість речовини, число частинок в якій рівне числу атомів у 12г ізотопу вуглецю 12С. Число молекул у молі будь-якої речовини однакове і називається сталою Авогадро; Кількість речовини
|

 , де
, де  – деяка функція.
– деяка функція.
 (з досліду).
(з досліду). можна виразити через її масу (m)
можна виразити через її масу (m)  або через число молекул (N)
або через число молекул (N) 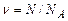 , де
, де  – молярна маса. Молярна маса пов’язана з масою однієї молекули
– молярна маса. Молярна маса пов’язана з масою однієї молекули