УРОВЕНЬ B
1. Найти массу метана (СН4), при полном сгорании которого до СО2(г) и Н2О(г) в тепловом агрегате выделяется теплота, достаточная для нагревания 1 л воды от 20 до 100оС. Мольную теплоемкость воды принять равной 75, 3 Дж/моль· К. КПД теплового агрегата составляет 50%.
РЕШЕНИЕ: Количество теплоты, необходимое для нагревания 1 л (1000 г) воды от 20 до 100оС определяем по формуле:
= = 334666, 7 Дж = 334, 7 кДж Определим массу метана при горении, которого выделяется такое количество теплоты. Процесс горения метана по условию задачи описывается уравнением: СН4(г) + 2О2(г) = СО2(г) + 2Н2О(г) Тепловой эффект этой реакции Dr.Ho(298K) определяем по I следствию из закона Гесса Dr.Ho(298K) = Df.Ho(298K, CO2(г)) + 2Df.Ho(298K, Н2О(г)) - - Df.Ho(298K, CН4(г)) - 2Df.Ho(298K, О2(г)) = (-393, 5) + 2(-241, 8) – - (-74, 9) = - 802, 2 кДж
Таким образом при сгорании 16 г метана выделяется 802, 2 кДж тепла. Определяем массу метана, при сгорании которой выделяется 334, 7 кДж теплоты. Составляем пропорцию: 16 г СН4 ― 802, 2 кДж
С учетом КПД теплового агрегата масса метана составляет
Ответ: масса метана составляет 13, 34 г. 2. Используя справочные данные по DfHo(298K, В) и So(298K, В), определить при каких температурных условиях возможно самопроизвольное протекание реакции Fe2O3(к) + 3Н2(г) = 2Fe(к) + 3Н2O(г)
РЕШЕНИЕ: Возможность самопроизвольного протекания реакции, определяется знаком перед величиной изменения энергии Гиббса для данной реакции: если Δ rG°(298К) < 0, самопроизвольное протекание реакции при стандартных условиях возможно в прямом направлении; если Δ rG°(298К) > 0, то при стандартных условиях прямая реакция невозможна, а возможна обратная реакция.. Значение Δ rG°(298К) рассчитываем по формуле: Δ rG°(298К) = Δ rН°(298К)·103 - Т Δ rS°(298К) где Δ rН°(298К) - изменение стандартной энтальпии реакции, кДж: Δ rS°(298К) - изменение стандартной энтропии реакции, Дж/К: 103 - пересчет кДж в Дж. Значение Δ rН°(298К) и Δ rS°(298К) определяем согласно первому следствию из закона Гесса: Δ rН°(298К) = [2Δ fН°(298К, Fe(к)) + 3Δ fН°(298К, Н2О(г))] – - [Δ fН°(298К, Fe2O3(к)) + 3Δ fН°(298К, Н2(г))]; Δ rS°(298К) = [2S°(298К, Fe(к)) + 3S°(298К, Н2О(г))] – - [S°(298К, Fe2O3(к)) + 3S°(298К, Н2(г))]; где Δ fН°(298К, В) и S°(298К, В) - стандартные энтальпии образования и энтропии веществ, значения которых находим из таблицы стандартных термодинамических величин.
Δ rН°(298К) = [2(0) + 3(-241, 84)] - [(-822, 2) + 3(0)] = 96, 68 кДж Δ rS°(298К) = [2·27, 15 + 3·188, 74] - [87, 4 + 3·130, 5] = 141, 62 Дж/К тогда: Δ rGо(Т) = 96680 - Т·141, 62 Ответ: При высоких температурах значение Δ rGо(Т) < 0 и, следовательно, реакция возможна при нагреве.
3. Рассчитать теплотворную способность каменного угля, если известно, что в нем содержится 80% углерода, а в отходящих газах после сгорания угля содержится 14% СО2 и 2% СО по объему.
РЕШЕНИЕ: Теплотворной способностью топлива называется тепловой эффект, который соответствует сгоранию единицы массы (1 кг) для твердых и жидких видов топлив (Qр, кДж/кг). Приводим уравнения горения углерода С(к) + О2(г) = СО2(г) (4.8) С(к) + ½ О2(г) = СО(г) (4.9) Из приведенных уравнений (ур. 4.8 и 4.9) следует, что масса сгоревшего углерода пропорционально объемам образовавшихся газов. Поскольку в каменном угле содержится 80% углерода, то в 1000 г каменного угля содержится 800 г углерода и в СО2 превратилось (ур 4.8)
а в СО превратилось: Исходя из того, что тепловые эффекты реакций (4.8) и (4.9) есть стандартные энтальпии образования СО2 и СО (величины табличные), но взятые с противоположным знаком, поскольку DН= - Qр DfНo(298 K, СО2) = - 393, 5 кДж/моль и DfНo(298 K, СО) = - 110, 5 кДж/моль рассчитываем количество теплоты, выделившейся при сгорании 700 г углерода до СО2 (ур. 4.8). Молярная масса углерода МС = 12 г/моль. При сгорании 12 г углерода выделяется 393, 5 кДж 700 г углерода выделяется Qр(4.8) кДж откуда: Qр(4.7) Рассчитываем количество теплоты, выделившейся при сгорании 100 г углерода до СО (ур.4.9). при сгорании 12 г углерода выделяется 110, 5 кДж 100 г углерода выделяется Qр(4.9) кДж откуда: Qр(4.9) Следовательно теплотворная способность каменного угля Qр = Qр(4.8) + Qр(4.9) = 22954 + 921 = 23875 кДж/кг
|

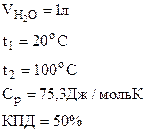
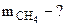


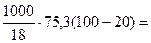

 ― 334, 7 кДж
― 334, 7 кДж г
г г
г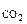 = 14% об.
ω
= 14% об.
ω  = 2 % об.
= 2 % об.
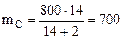 г углерода,
г углерода,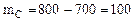 г углерода (ур. 4.8)
г углерода (ур. 4.8) кДж
кДж кДж
кДж


